Modalități de neutralizare a amoniacului în organism
Țesutul este preferabil NH amoniac sub formă de ioni de amoniu în echilibru cu concentrația neîncărcat mică de amoniac.
1.Vosstanovitelnoe aminare.
O modalitate de legare și neutralizarea amoniacului din organism, in special in creier, retina, rinichi, ficat și mușchi - biosinteza amide ale acizilor glutamic și aspartic (glutamină sau asparagină):
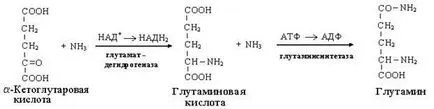
Această reacție are loc în multe țesuturi, dar cel mai important pentru sistemul nervos, în special sensibili la efectele toxice ale amoniacului. Prima reacție este o reacție de solicitare glutamatdegidrogenaznoy (revers oxidativ dezaminare KLH).
neutralizare prin glutamină sinteza amoniacului are o importanta anabolic deoarece glutamina este utilizat pentru a sintetiza o serie de compuși. În primul rând, trebuie remarcat faptul că glutamina - unul dintre cei 20 de aminoacizi care fac proteine. Mai mult, gruparea amidă a glutaminei utilizată în sinteza asparagina, glucozamină și alte aminozaharuri, purina și nucleotide pirimidinice. Astfel, în aceste reacții, azot amoniacal este inclus într-o varietate de componente structurale și funcționale ale celulei.
Glutamina poate apoi introduce toate țesuturile, în care hidroliza se efectuează cu participarea glutaminaza sale:
În mod similar, formarea de asparagina (prin stiuca).
2. Formarea de săruri de amoniu.
Excreția de amoniac în urină normale mici - aproximativ 0,5 grame pe zi. Dar este de mai multe ori crește cu acidoza, t. E. Cu creșterea conținutului de acid în organism. Amoniacul este produsă în rinichi datorată în principal gruparea amidă a glutaminei. Glutamina glutaminaza hidrolizat fosfat activat, prezentă în celulele epiteliale ale tubilor renali. O parte din amoniacul (circa 30%) produs de cealaltă - ca rezultat al dezaminarea indirect al aminoacizilor.
Acidul rezultat neutralizeaza amoniacul: NH3 + H + → NH4 +. Amoniacul neîncărcată și acidul din celulele sunt în echilibru cu formele lor ionizat. Patrunde prin membranele celulare de acid predominant neionizată și amoniac și în lumenul tubilor renali (m. E. Deja în urină) amoniac accepta un proton de acid, pentru a forma o sare de amoniu. care este eliminat din organism. excreția renală a amoniacului servește pentru a obține exact de acid în loc de azot, așa cum este indicat de o rată semnificativă de excreție cu acidoza, mică - normală aciditate fluid interstițial și sânge, și nu excreția de amoniac la alcaloză. În același timp, acest proces asigură păstrarea corpului ionilor de Na +, care, în absența ionilor de amoniu la anioni derivați din acizi. Pierderea acestor cantități de Na +, care sunt necesare pentru îndepărtarea acidului acidozei, ar determina o scădere a presiunii osmotice a fluidului intercelular și sânge și prin aceasta la reducerea volumului de fluid interstițial, m. E. Tissue deshidratare.
3. Mecanismul principal de amoniac de legare în organism este sinteza ureei. Ureea excretat prin urină ca produs final major al proteinelor, amino metabolismul acidului respectiv. Conturile Uree pentru 80-85% din azotul total evacuat din organism. Cantitatea de uree eliberată depinde de cantitatea de proteine care provin din alimente. Dacă rația zilnică cuprinde 80-100 grame de proteine, apoi formate și excretată 25-30 g de uree pe zi.
Site-ul principal al sintezei ureei este ficatul. Sinteza unui proces ciclic metabolic ureei și se numește ciclul ornitin Krebs formarea ureei (ciclul ureei Krebs - Henzelyayta).
În prima etapă de NH3 și CO2, cu participarea ATP sintetizat compusi de energie karbamoilfosfat:
În a doua etapă de formare a ureei ciclu karbomoilfosfata de condensare are loc pentru a forma ornitină și citrulină. În etapa următoare legarea unei prime molecule de NH3 prin aminare reductivă pentru a forma (cu cheltuielile de molecule ATP) acid aspartic. Apoi citrulină și acidul aspartic reacționează pentru a forma acidul argininosuccinic. care descompune în arginină și fumarat implicând argininosuktsinatliazy. Arginina este scindată de către enzima arginază ornitină și uree.
Ornitina rezultată poate intra în formarea ciclului ureei următor. In timp ce arginina este prezentă în toate celulele umane, formarea ureei are loc exclusiv în celulele hepatice - un singur corp, unde localizate enzima arginase. Ureea din celulele hepatice in sange si excretat prin rinichi.
Pentru sinteza unei molecule de uree este nevoie de două molecule de NH3, o moleculă de CO2 și trei molecule de ATP.
astfel bazate pe date reale privind mecanismele de neutralizare a amoniacului din partea corpului a amoniacului este utilizat în biosinteza aminoacizilor prin aminarea reductivă a acizilor a-ceto prin mecanismul reacției transaminare. Amoniacul este legat în biosinteza de glutamină și asparagină. O cantitate de amoniac este excretat prin urină sub formă de săruri de amoniu. Forma creatinină, care este format din creatina si fosfocreatina, excretate o mare parte azot amino. Cea mai mare cantitate de amoniac consumat în sinteza ureei, care este excretat în urină ca produs final principal al metabolismului proteic la oameni și animale.