Disport® medicamente de uz utilizator Liofilizat, analogi, comentarii
Instrucțiuni de utilizare a medicamentului DISPORT® (DYSPORT®)
NUMĂR DE ÎNREGISTRARE: LP 001486-080212
TRADE NUME: Disport®
INN sau NUME grupare: Complex toxină botulinică de tip A - hemaglutinina
FORMA DE DOZARE: Liofilizat pentru soluție injectabilă
INGREDIENTE
Substanța activă: Un flacon conține
Complexul de toxină botulinică de tip A - hemaglutinina 300 UI *
excipienţi:
albumină umană 125 pg
Lactoză 2,5 mg
* Unitate ED a activitatii societatii.
grupa farmacoterapeutică
acționează periferic relaxant muscular
codul ATC: M03AH01
EFECTE BIOLOGICE
Principiul activ este o toxină botulinică de tip Clostridium - A, care blochează eliberarea de acetilcolină la nivelul joncțiunii neuromusculare, având ca rezultat eliminarea spasme musculare în administrarea medicamentului. Recuperarea transmisiei impulsurilor nervoase are loc treptat, pe măsură formarea de noi terminații nervoase și a restabili persoanele de contact cu
Motor endplate postsinaptici.
INDICATII
Tratamentul blefarospasm, spasmului hemifacial, torticolis spasmodic, spasticitatea mâinilor după un accident vascular cerebral, riduri hiperkinetice (riduri de expresie) adulți facial.
Tratamentul deformare dinamică cauzat spasticitate la copiii cu paralizie cerebrală cu vârsta de 2 ani.
Tratamentul hiperhidrozei axilare zona.
CONTRAINDICAȚII
Disport® este contraindicat în timpul sarcinii și în timpul alăptării.
In bolile acute administrarea medicamentului se efectuează după recuperare.
Disport® contraindicat la pacienții cu hipersensibilitate la una din componentele preparatului.
Mod de administrare
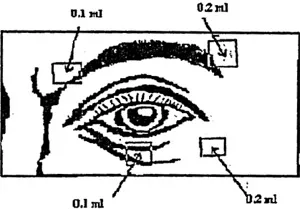
Doza totală poate fi redusă la 500 UI pentru a preveni excesivă slăbiciune musculară injectabil în cazurile când mușchiul țintă al pacientului este mic în volum, atunci când este injectat în mușchi BB nu este introdus sau când injectarea pacienților se face în mai multe puncte ale unui mușchi. Ameliorarea clinica are loc în decurs de două săptămâni după injectare. Injecțiile pot fi repetată la fiecare aproximativ 16 săptămâni, sau după cum este necesar pentru a menține efectul, dar nu mai des decât o dată la 12 săptămâni.
Reguli pentru prepararea soluției. injecție
Cu sticla îndepărtat capacul de plastic protector al primei deschideri de control. La o diluare a medicamentului nu poate deschide o sticlă prin scoaterea fișei. Imediat înainte conținutului flaconului de diluare partea centrală a dopului să fie tratat cu alcool. Liofilizatul este diluat prin injectarea în flaconul cu un volum reglementat de soluție de clorură de sodiu 0,9% pentru injecție prin puncție sterilă ac plutei calibrul 23 sau 25. Soluția rezultată este un lichid transparent, incolor. Deoarece medicamentul nu conține un conservant, este recomandabil să-l utilizați imediat după reconstituire. Singur medicament nu poate fi depozitat timp de mai mult de 8 ore, la o temperatură cuprinsă între 2 ° și 8 ° C
Precautii
Tratamentul medicamentos trebuie să fie efectuate de către experți cu experiență în diagnosticarea și tratamentul unor astfel de condiții, și instruit pentru a efectua un tratament.
Cu extremă precauție trebuie readministrat medicamentului la pacienții care au marcat o reacție alergică la o injecție anterioară.
Acesta a fost raportat efecte secundare care rezultă din acțiunea toxinei asupra musculaturii la distanță de locul de administrare (vezi. „Efect secundar“ secțiune). Pacienții care au primit Disport® in doze terapeutice pot prezenta slăbiciune musculară generală. Riscul unor asemenea efecte secundare pot fi reduse, sub rezerva recomandărilor pentru formularea de dozare și aplicarea dozei minime eficiente a medicamentului.
Cu grijă și sub supraveghere medicală strictă ar trebui să utilizeze medicamentul la pacienții cu semne clinice sau subclinice ale leziunilor transmisiei neuromusculare (de exemplu, miastenia gravis). Astfel de pacienți pot avea sensibilitate crescută la preparate de toxina botulinica, care le poate provoca slăbiciune musculară pronunțată.
Măsuri de precauție ar trebui Disport® administrat pacienților cu inghitire redusă și de respirație, deoarece datele de încălcare pot fi exacerbate datorită acțiunii toxinelor pe scară largă asupra mușchiului corespunzător.
La pacienții care suferă de boli respiratorii cronice, în cazuri rare, se poate dezvolta aspirație.
Pe fondul terapiei de toxina botulinică de tip A sau B, au fost raportate câteva cazuri de deces cauzate de disfagie (inghitire tulburare), pneumopatie sau la pacienți cu astenie severă.
Pacienții și cei care le îngrijesc trebuie să fie avertizat de necesitatea urgentă de a vedea un medic, în caz de orice încălcare a deglutiție, de vorbire, și tulburări respiratorii.
formarea de anticorpi protivobotulinicheskih observată la o minoritate de pacienți supuși terapiei Disportom®. Clinic se constată o scădere manifestată în efectul terapeutic, care a necesitat doze constante de creștere ale medicamentului.
La pacienții cu timpul de coagulare întârziată și inflamație la locul propus de injectare, Disport® trebuie aplicate în caz de necesitate extremă.
Notă: Atunci când atribuirea Disporta® trebuie remarcat faptul că unitatea de droguri sunt specifice și nu pot fi comparate cu cele ale altor medicamente care conțin toxina botulinica.
EFECTE ADVERSE
In timpul diferitelor studii clinice cu droguri Disport® implicat aproximativ 7800 de date pacienților privind incidența reacțiilor adverse au fost colectate, care au următoarea clasificare: foarte frecvente (≥1 / 10), frecvente (≥1 / 100 - <1/10), нечасто (≥1/1,000 до <1/100), редко (<1/1,000), очень редко (≥1/10,000).
Reacții adverse frecvente:
Din sistemul nervos
Rare: amiotrofia nevralgică.
Afecțiuni cutanate și ale țesutului subcutanat
Mai puțin frecvente: iritație. Injecțiile pot fi însoțite de o senzație de arsură, care durează 1-2 minute.
Rare: erupții cutanate.
Reacțiile generale și locale
Frecvente: slăbiciune generală, oboseală, simptome asemănătoare gripei, durere și hematom la locul de injectare.
Spasticitate mână la adulți după accident vascular cerebral
In 14 studii clinice care au implicat 141 pacienți au fost raportate următoarele reacții adverse:
În partea a tractului gastro-intestinal:
Frecvente: disfagie.
Pe partea sistemului musculo-scheletice și țesutului conjunctiv:
Adesea, muschii bratului slăbiciune.
Trauma și complicații ale procedurilor:
Frecvente: răniri accidentale / toamna.
Disfagie a fost înregistrată atunci când dozele au fost mai mari de 2700 UI angajate introdus într-un punct sau mai multe puncte repartizate între administrare.
deformare picior dinamică datorită spasticitate la copiii cu paralizie cerebrală
In 14 studii clinice care au implicat 900 de pacienți au fost raportate următoarele reacții adverse:
În partea a tractului gastro-intestinal:
De multe ori diaree.
Pe partea sistemului musculo-scheletice și țesutului conjunctiv:
De multe ori slăbiciune a mușchilor picioarelor.
Rinichii si sistemul urinar:
Frecvente: incontinență urinară.
Reacțiile generale și locale
Frecvente: tulburări de mers.
Trauma și complicații ale procedurilor:
Frecvente: răniri accidentale datorate căderilor.
rănire accidentală din cauza căderii și mers anormal poate fi o consecință a slăbiciunii musculare excesive și / sau proliferarea acțiunii toxinei „la alta, vecine locul injectării, mușchii implicați sau implicați într-un act cu motor în menținerea echilibrului pacientului în picioare și mersul pe jos.
torticolis spasmodic
21 Într-un studiu clinic care implica 4100 de pacienti cu privire la următoarele reacții adverse au fost raportate:
Din sistemul nervos:
Frecvente: disfonie.
Mai puțin frecvente: dureri de cap.
De la un organ vedere:
Mai puțin frecvente: diplopie, tulburări de cazare.
Modificări ale sistemului respirator, toracice și mediastinale:
tulburări respiratorii: Rare.
În partea a tractului gastro-intestinal:
Foarte frecvente: disfagie.
Mai puțin frecvente: senzație de gură uscată.
efectul disfagia este dependentă de doză și apare cel mai frecvent atunci cand este administrat medicamentul, în mușchiul sternocleidomastoidian. Poate fi necesar un regim alimentar cu excepția roughage până la dispariția simptomelor.
Blefarospasm și spasm hemifacial
In 13 studii clinice care au inclus aproximativ 1400 de pacienți au fost raportate următoarele reacții adverse:
Din sistemul nervos:
De multe ori slăbiciune a mușchilor faciali.
Mai puțin frecvente: pareza mușchilor faciali.
De la un organ vedere:
Foarte frecvente: ptoza.
Frecvente: diplopie, ochi uscat mucoasei, lacrimare.
Rare: oftalmoplegia.
Afecțiuni cutanate și ale țesutului subcutanat
Frecvente: umflarea pleoapelor.
Rare: volvulus secol.
pot să apară efecte secundare atunci când normele de non-conformitate medic efectuarea injectării (diluție calcularea corectă a dozei administrate, administrarea o alegere corectă a punctelor de pe direcția acului și inserția adâncimii) și difuzia excesivă asociată a medicamentului și o paralizie temporara a grupelor musculare adiacente la locul injectării.
axilar hiperhidroza
au fost raportate în 4 studii clinice care au inclus aproximativ 217 de pacienți următoarele reacții adverse:
Afecțiuni cutanate și ale țesutului subcutanat
Frecvente: transpirație Compensatorii.
riduri hiperkinetic (riduri) ale persoanei
Următoarele reacții adverse (de obicei, ușoare până la intensitate moderată) au fost înregistrate în cererea Disporta® pentru ridarea facial de hiperkinetic:
De la un organ vedere:
Frecvente: umflarea pleoapelor și conjunctivei.
Mai puțin frecvente: mucoasa ochiului uscat (keratoconjunctivita sicca).
Reacțiile generale și locale
Foarte frecvente: reacții la nivelul locului de injectare (incluzând durere, hematom, prurit, parestezii, eritem, erupții cutanate, care este adesea observată în grupul placebo).
Pe partea sistemului musculo-scheletice și țesutului conjunctiv:
De multe ori slăbiciunea adiacente la locul introducerii de mușchi care de multe ori duce la ptoză, pleoapelor, astenopie (oboseala ochilor) sau, mai rar, o pareză a mușchilor faciali și tulburări de vedere.
Din sistemul nervos:
Foarte frecvente: dureri de cap (la fel de des observate în grupul placebo).
Afecțiuni cutanate și ale țesutului subcutanat
Mai puțin frecvente: erupții cutanate, prurit.
Rare: urticarie.
Experiența post-înregistrare
Cele mai multe reacții adverse sunt ușoare și tranzitorii.
slăbiciune musculară severă, disfagie, pneumonie de aspirație care pot fi fatale, sunt foarte rare, cu o frecvență de 1 la 10000 (a se vedea. „Atenționări și precauții“ secțiune). tulburări digestive Foarte rar (diaree), reacții alergice cutanate, amețeli și dureri de cap.
SUPRADOZĂ
Utilizarea unor doze mari poate duce la slăbiciune musculară generalizată. Paralizia mușchilor respiratori este necesar să se efectueze ventilație mecanică. În supradozajul administrarea antitoxina (ser protivobotulinicheskoy) este oportun pentru primele trei ore. In general, tratamentul este direcționat supradozajul terapia generală de întreținere cu monitorizarea constantă a pacienților.
Interacțiune cu alte medicamente
Agenți care acționează asupra transmisiei neuromusculare, cum ar fi antibiotice aminoglicozidice, trebuie utilizat cu precauție.
Aplicarea sarcinii și în timpul alăptării
Teratogenitate și alte studii de reproducere Disportom® a fost realizat. aplicații de securitate Disporta® la femeile gravide și care alăptează nu au fost confirmate.
IMPACTUL ASUPRA CONDUS AUTOVEHICULE ȘI UPRAVLENIEMEHANIZMAMI
INSTRUCȚIUNI DE PRELUCRARE REZIDUURI Soluțiile medicamentoase
Imediat după injectare rămasă în soluția de flacon sau seringă trebuie inactiva soluție de hipoclorit de sodiu care conține 1% clor activ. Toate materialele de suport care au fost în contact cu produsul trebuie să fie eliminate în conformitate cu practica standard de spital. preparare deversat trebuie șters cu o cârpă absorbantă îmbibat în soluție de hipoclorit de sodiu 1%.
AMBALARE
Liofilizatul pregătit pentru soluție injectabilă.
300 UI într-un flacon din sticlă, închis cu un dop de cauciuc acoperit cu aluminiu lustruirea cu o gaură de ac în centru și capacul închis plastic protector al primei deschideri de control.
1 flacon este fixat în suportul de hârtie, împreună cu instrucțiunile de utilizare, introduse în ambalaj din carton.
Depozitare și transport
Depozitarea și transportul tuturor tipurilor de transport acoperite la 2 până la 8 ° C
A nu se congela!
A nu se lăsa la îndemâna copiilor.
Dysport este stocată într-un închis separat caseta marcată într-o instalație de frigider în cazul în care efectuează injectarea medicamentului.
Dysport nu ar trebui să fie acordat în stocarea pacientului.
VALABILITATE
2 ani.
A nu se utiliza după data de expirare înscrisă pe ambalaj.
CONDIȚIILE DE DISEMINARE
Medicamentul este eliberat, depozitat și aplicat numai în instituții specializate.
PRODUCĂTOR
Ipsen Biopharm Ltd.
Ash Road, Wrexham Industrial Estate,
Wrexham LL13 9UF, Marea Britanie.