Valorile densității de alcool și exemple de sarcini
Metanol, etanol și propanol sunt miscibili cu apa în orice proporție. Odată cu creșterea masei moleculare a alcoolului solubilitatea în oda scade brusc. alcooli superiori sunt practic insolubile în apă.
alcooli inferiori au un miros specific de alcool, mirosul de mijloc puternice și omologi adesea neplăcute. alcooluri superioare nu au practic nici un miros. alcooli terțiari mucegai au un miros caracteristic special.
glicoli inferiori - lichid vâscos incolor, inodor; ușor solubil în apă și etanol, au un gust dulce.
Alcoolii au puncte de fierbere anormal de mare în comparație cu clasele de compuși organici, cum ar fi alcani, halogenclorură, tioli, amine. De exemplu, punctul de fierbere al etanolului 78 o. întrucât cloretan - 13 o C și etan - 88.5 ° C. Aceste diferențe se datorează caracteristici alcooli structurali.
Compoziția chimică și densitatea alcoolului
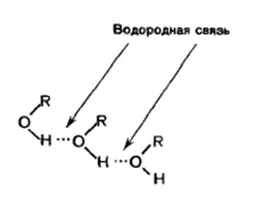
un atom de oxigen în molecula de alcool are electronegativitate ridicată și trage densitatea s-electron a legăturilor asociate atomi, în particular un atom de hidrogen. Comunicare O-H în molecula de alcool este puternic polarizat R → O ← H. Densitatea de electroni a atomului de hidrogen este redus. Prin urmare, se poate interacționa cu perechea de electroni unshared atomului de oxigen al altei molecule de alcool. Intre doua molecule are loc legături de hidrogen non-covalent (legăturii de hidrogen ilustrează grafic punctele făcute). Molecule legate prin legături de hidrogen la asociați formă: