Valence de FeCl2 clor, felc3, ce distractiv!
Valence este capacitatea celulelor de a atașa la alte elemente.
Aceasta este, valența -. Numărul care prezintă o serie de elemente care se poate fixa la atomul particular. Determinată de numărul de electroni nepereche excitat și atomii neexcitat.
Clorul este un element al șaptelea podrugppy grup principal, a treia perioadă a sistemului periodic al elementelor chimice. Numărul atomic de clor - 17. se scrie pe ambele CI Chlorum. Clorul este partea activă a grupării metaloid și halogen.
Valența și oxidarea atomilor de clor în molecula sa

Oxidarea desemnată numeric în starea atomului în compus. este, de asemenea numit numărul de oxidare. Determinarea care credea în mod convențional ca un simplu compuși covalenți valoarea puterii pozitivă este egal cu numărul de elemente de oxidare extrase din perechea de electroni de legare atom, și o valoare negativă gradul de oxidare - numărul de perechi de electroni pull. Prin urmare, determinarea gradului de oxidare, se consideră că compușii constau numai ionii de încărcate pozitiv și negativ.
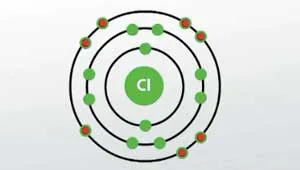
Vorbind de clor, valență și oxidarea starea în moleculă, următoarele valori:
- Valence a - 1.
- Gradul de oxidare - 0
Este valență azot siliciu fosfor
Care este valența altor substanțe, de multe ori interacționează cu clor?
- Valența azotului. Azotul din tabelul periodic reprezentat de litera N. Se poate acce creaturi sub formă de diferite valență în funcție de compus. Se întâlnește chiar și valența fracționată. Este perfect posibil să se uite la exemplul de oxidare de azot: N2O - monovalent de azot (gaz ilariant) NO - bivalent. NO2 (dioxid de azot, gaz brun). Compușii cu azot, în stare de oxidare 5 - oxid nitric (V) N2O5, acid azotic și sărurile sale - nitrați, și colab.
Cu toate acestea, valența azotului = 3.
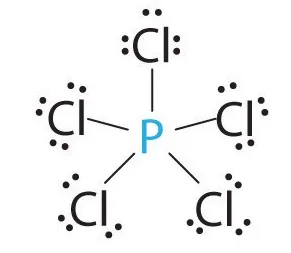
- Fosforul (P) este în treia perioadă, grupa V, principalele subgrupe ale sistemului periodic Mendeleev. valență de fosfor poate fi, de asemenea, diferite, totul, la fel ca orice altă substanță, se bazează, de fapt, cu orice substanță chimică se întâmplă obligațiuni de fosfor. Cu toate acestea, valența fosforului este samog III, V.
- Siliciul (Si) - este un 3-perioadă, grupa IV din subgrupul principal al sistemului periodic. Valenței - 2, 4.
Valența clor în compuși organici, în stare excitată în acid clorhidric, în oxidul superior
Valenței clorului din compuși organici pot fi diferite, în funcție de fapt de compus.
Reacția principală a clorului cu substanțe organice:
- C compușii saturați:
CH3-CH3 + Cl2 → C2H5Cl + HCI
- Se alătură compușilor nesaturați la legături multiple:
CH2 = CH2 + Cl2 → CI-CH2-CH2-CI
- Compușii aromatici substituiți cu un atom de hidrogen cu clor, în prezența unui catalizator (de exemplu, AlCl3 sau FeCl3):
C6H6 + Cl2 → C6H5Cl + HCI
In starea undriven la nivel energetic atom de clor de 3 este 1 electron nepereche este astfel neexcitat atom de clor poate arăta valență 1.
În stare excitată - valență 3.
oxid superior este un oxid care elementul prezintă un grad ridicat de oxidare.
Cl2O7 - oxid de clor (VII) - Art. oxidat. CI (+7) - oxid principal.
clor valenței cu metale, fosfor, argint, sodiu, hidrogen, oxigen, calciu, aluminiu, cu un nemetale, cu fier
În general, valența - unul dintre subiectele cele mai complexe în chimie să-l dau seama, au o mulțime de materiale pentru a citi cu atenție. Necunoscând legile și regulile de bază ale chimiei, nimeni nu poate înțelege ce este cu valența, cu atât mai puțin să învețe cum să-l identifice.
Interacțiunea cu metale:
Clorul reacționează direct cu practic toate metalele, cu toate acestea, pentru anumite reacții necesită umiditate sau căldură.
Interacțiunea cu nemetale:
nemetale C (cu excepția de carbon, azot, fluor, oxigen și gaze inerte) formează un cloruri corespunzătoare.
În diverși compuși din diferite valență în clor, cu metale (argint, sodiu, fier, aluminiu) valență clor = 1, cu nemetale având o valență diferită, dar, cel mai adesea, de asemenea 1. în compușii cu acid clorhidric valență = 1.
În general, CL are întotdeauna o valență de 1, combinarea cu substanțe excepții sunt substanțe cu o valență VII.