Reglarea metabolismului lipidic
factori. În special, rata sintezei de reductaza in ficat este supus unei variații diurn clar: maxim este miezul nopții, iar cea minimă - dimineața.
Activitatea HMG-reductazei este crescută după administrarea de hormoni tiroidieni și insulină. Aceasta conduce la sinteza crescută a colesterolului și o creștere a nivelului acestuia în sânge.
Când jeun, tiroidectomie, glucagon, și contrast glucocorticoizi, marcat inhibarea sintezei colesterolului, care se datorează în primul rând o scădere a activității de HMG-CoA reductază.
metabolismul lipidic este reglată de sistemul nervos central. cortexul cerebral are un efect asupra trofică tesutul adipos sau prin diviziile inferioare ale SNC - sistemul simpatic și parasimpatic, fie prin glandele endocrine. În prezent, acesta a stabilit o serie de mecanisme biochimice care stau la baza acțiunii hormonilor asupra metabolismului lipidelor.
ARNm sinteza inhibitorilor. În plus, este cunoscut faptul că efectul hormonului de creștere asupra lipolizei se caracterizează printr-o fază de latență care durează aproximativ 1 oră, în timp ce adrenalina stimulează lipoliza aproape instantaneu. Cu alte cuvinte, se poate presupune că efectul principal al acestor două tipuri de hormoni asupra lipolizei manifestată în diferite moduri. Adrenalină stimulează activitatea adenilat ciclazei și hormonul de creștere induce sinteza enzimei. Mecanismul specific prin care GH crește selectiv sinteza adenilat ciclazei, este încă necunoscut.
Insulina are efectul opus de adrenalină și glucagon asupra lipolizei și mobilizarea acizilor grași. Recent, sa demonstrat că insulina stimulează activitatea fosfodiesterazei în țesutul adipos. Fosfodiesteraza joacă un rol important în menținerea unui nivel constant de AMPc în țesuturi, prin urmare, creșterea conținutului de insulină ar trebui să crească activitatea fosfodiesterazei, în care, la rândul său, duce la o scădere a concentrației cAMP în celulă, și, prin urmare, la formarea formei active a lipazei.
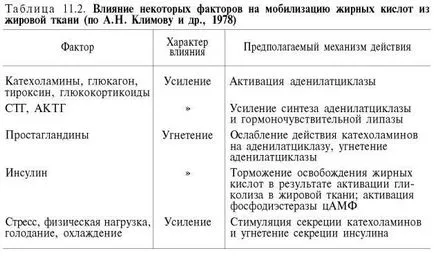
Fără îndoială, alți hormoni, cum ar fi tiroxina, hormoni sexuali, de asemenea, afecta metabolismul lipidelor. De exemplu, este cunoscut faptul că îndepărtarea gonade (castrare) provoacă la animale depunerea excesivă de grăsime. Cu toate acestea, informațiile pe care nu le-am furnizat încă baza de a vorbi cu încredere despre mecanismul specific al acțiunii lor asupra metabolismului lipidelor. Tabel. 11.2 rezumă impactul mai multor factori privind mobilizarea acizilor grași din depozitele de grăsime.
tulburări ale metabolismului lipidic
Perturbarea în absorbția de grăsime. Tulburări ale metabolismului lipidic poate fi deja în procesul de digestie și absorbție a grăsimilor. Un grup de tulburări asociate cu un aport insuficient de lipazei pancreatice în intestin, iar al doilea este ca urmare a încălcării veniturilor în intestin de bilă. Mai mult decât atât, descompunerea proceselor de digestie și absorbție a lipidelor poate fi asociată cu boli ale tractului digestiv (enterite, hypovitaminosis și anumite alte condiții patologice). monogliceride și acizi grași formați în lumenul intestinal nu poate fi în mod normal absorbite datorită deteriorării epiteliale intestinale foaie. În toate aceste cazuri, scaun conține o mulțime de grăsime sau de acizi grași nevsosavsheysya mai mari nedivizați, și are o culoare gri-alb caracteristic.
Violarea proceselor de tranziție a grăsimii din sânge în țesut. Cand activitatea lipazei insuficienta lipoprotein din sange este perturbat de acizi grași de tranziție de la chilomicronilor (XM) în plasma din sânge depozite de țesuturi grase (nu clivat trigliceride). Cel mai adesea este o boala ereditara cauzata de lipsa completă a activității lipoprotein lipazei. Plasma de sânge, astfel,
Are o culoare lăptoasă, ca urmare a conținutului extrem de ridicat al XM. Cel mai eficient tratament pentru aceasta boala este inlocuirea uleiurilor naturale care conțin acizi grași având 16-18 atomi de carbon, de sinteză, care includ acid gras cu catenă scurtă având 8-10 atomi de carbon. Acești acizi grași pot fi absorbite din intestin în sânge direct, fără XM formarea prealabilă.
În prezent, fenomenul cetonemiei și cetonuriei în diabetul zaharat sau de foame poate fi explicată după cum urmează. Și diabet și înfometarea sunt însoțite de o reducere drastică a depozitelor de glicogen în ficat. Multe țesuturi și organe, cum ar fi tesutul muscular, sunt într-o stare de foame de energie (cu o lipsă de insulină, glucoza nu poate
viteză suficientă pentru a intra în celulă). În această situație, din cauza excitarea centrelor metabolice în impulsurile sistemului nervos central de la celulele Chemoreceptors,, lipoliza îmbunătățită dramatic energivore și mobilizarea unui număr mare de acizi grași de la depozitele de grăsime în ficat. Ficatul este o formare intensivă a corpilor cetonici. Rezultând într-o cantitate neobișnuit de mare de corpilor cetonici (acid acetoacetic și β-hidroxibutiric) sunt transportate prin fluxul sanguin de la ficat la țesuturile periferice. țesut periferic în timpul înfometare și diabetul păstreze capacitatea de a utiliza corpilor cetonici ca material energetic, ci datorită concentrației neobișnuit de mare a corpilor cetonici în sânge care curge în mușchi și alte organe nu pot face față cu oxidarea lor și ca o consecință acolo cetonemie.
Ateroscleroza și lipoproteine. În prezent, sa dovedit a fi rolul principal de clase specifice de lipoproteine în patogeneza aterosclerozei. Poziția cunoscută Acad. NN Anicikov „fără colesterol nu ateroscleroza“, cu cunoștințele actuale pot fi exprimate într-un alt mod: „fără a lipoproteinelor aterogene poate fi ateroscleroza.“
Să ne amintim că lipoproteinelor plasmatice - compuși complecși sunt complexe, în care structura, în plus față de proteine, include o componentă lipidică. Lipoproteinele plasmatice sunt structura caracteristică: în interiorul particulelor de lipoproteine este picătură de ulei (miez) care conține lipide nepolare (trigliceride, colesterol esterificat). Picăturii de grăsime, înconjurat de o membrană, care cuprinde fosfolipide, colesterol si proteine. Grosimea acestui înveliș este 2,0-2,5 nm, care corespunde cu jumătate din grosimea bistratul fosfolipidic a membranei celulare.
Există mai multe clase de lipoproteine: alfa-lipoproteine și lipoproteine cu densitate mare (HDL); P-lipoproteine sau lipoproteine cu densitate joasă (LDL); pre-β-lipoproteina sau lipoproteine cu densitate foarte mică (VLDL); chilomicroni (CM).
Sa stabilit că ateroscleroza și bolile asociate apar cu o creștere semnificativă a fracțiunilor LDL plasmatice din sânge, și în multe cazuri, și fracțiile VLDL (vezi cap. 17).
Cercetările din ultimii 5 ani au aratat ca pe propria lor LDL nativă și VLDL alergenicitate nu posedă. lipoproteine aterogenă în aceste clase apare numai atunci când particulele lor suferă modificări chimice și, mai presus de toate peroxidarea. In acest prim astfel de produse sunt produse în compoziția lor