Proteine - electroliti amfoteri Yermolaev 1974 m
Proteine - electroliti amfoteri
Studiind compoziția chimică a proteinei s-a constatat că, în molecula sa există amină liberă (NH2) și grupări carboxi (COOH), care sunt în soluție sub formă de NH3 și COOH. Prin urmare, în soluția de proteine au proprietăți amfotere (ampholyte, Amphion). Când se trece curent electric proteine se va deplasa, în funcție de sarcina moleculelor de proteină la catod sau anod (Fig. 10).
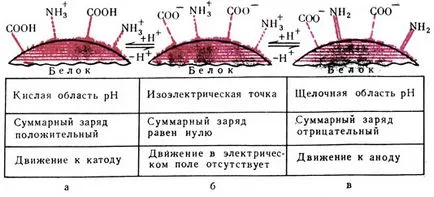
Fig. 10. Proteine - compus amfoter. și - într-o soluție acidă, încărcătura totală a proteinei și proteina devine un cation pozitiv; b - punctul izoelectric; încărcătura totală a moleculei de proteină este egală cu zero; în - într-un mediu alcalin suprimat disocierea grupărilor aminice. Acuzația a moleculelor de proteine este negativ și proteina se deplasează la anod (anion are rolul de proteine)
În soluții alcaline, proteina acționează ca anion: de exemplu, există o pierdere de H + NH + 3 prin acțiunea hidroxidului de sodiu.
În soluții acide, dimpotrivă, proteina acționează ca un cation, ca și în cazul acidului clorhidric:
Astfel, determinantul comportamentul proteinei ca un anion sau cation este concentrația de ioni de hidrogen sau pH-ul mediului. Atunci când concentrația ionilor de hidrogen (mediu de acid - pH 0-7), proteina devine cation când este coborât (miercuri schelochnaya- pH 7 -14), dimpotrivă, particulele de proteine devin anioni. O astfel de capacitate de proteină sau prezintă proprietăți acide sau alcaline se caracterizează drept compus amfoter.
Cu toate acestea, în anumite valori ale pH-ului numărul de sarcini pozitive ale proteinei va fi egal cu numărul de sarcină negativă și molecula ca întreg este aproape egal cu zero. Molecula de proteină nu se va muta într-un câmp electric. În aceste condiții, proteina este în starea izoelectrică; pH-ul soluției, în care proteina este in stare izoelectric se numește punctul izoelectric. Punctul izoelectric al mai proteine naturale se află într-un mediu slab acid (pH 4.8-5.4). Molecula de astfel de proteine conține mai multe grupări carboxil decât amino. Acest lucru indică faptul că în compoziția lor conține aminoacizi mai dicarboxilici (vezi. Aminoacizii). Punctul izoelectric al proteinei este în stare puțin stabilă și cu mici modificări ale pH-ului în partea acidă sau alcalină precipită cu ușurință.
Proteinele amfoteri sta la baza sistemului tampon de proteine, care este implicată în menținerea mediului de reacție special de sânge. Proprietățile amfoteri ale proteinelor sunt folosite pentru a le separa în fracții separate (metoda electroforeză), în scopul de a diagnostica boli diferite și să monitorizeze starea pacientului.