Formula primei legi a termodinamicii
Legile de bază, care stau la baza termodinamicii, numite începuturi. Baza termodinamicii sunt trei principii. Prima lege a termodinamicii este legea de conservare a energiei pentru procesele termodinamice. În formă integrată, cu formula primei legi a termodinamicii arata ca:
ceea ce înseamnă că cantitatea de căldură furnizată în sistem termodinamic, este de a face acest sistem, și schimbarea energiei sale interne. Sa convenit să ia în considerare faptul că în cazul în care căldura este furnizată în sistem, este mai mare decât zero (), iar în cazul în care activitatea se face de la sine sistem termodinamic, atunci este pozitiv ().
Prima lege a termodinamicii pot fi scrise în formă diferențială, atunci formula pentru ea este:
în care - o cantitate infima de căldura furnizată în sistem; - sisteme de lucru elementare; - o mică schimbare în energia internă a sistemului.
În cazul în care studiul de sistem termodinamic este un gaz ideal, operația efectuată de către acestea este legată de schimbarea volumului (), caz în care prima lege formula termodinamicii (în formă diferențială) poate fi considerată expresia:
Trebuie amintit faptul că prima lege a termodinamicii nu indică direcția în care are loc procesul termodinamic. Formula prima pornire arată doar parametrii sistemului de schimbare, în cazul în care are loc procesul. În termodinamică, pentru a evidenția direcția procesului corespunde celui de al doilea principiu.
Formula primei legi a termodinamicii pentru procese
Să presupunem că toate aceste procese continuă să aibă loc într-un gaz ideal.
Pentru un proces care are loc într-o masă de gaz la temperatură constantă (proces izoterma), prima lege formula termodinamicii se transformă în:
Din expresia (4) că toată căldura primită de sistemul termodinamic, este cheltuit pentru a face acest sistem.
Formula primei legi a termodinamicii pentru procesul izocoră este expresia:
Atunci când procesul de izocoră, tot sistemul rezultat de căldură este de a crește energia internă.
Procesul de izobară Legea întâi formula termodinamicii rămâne neschimbată (3).
proces adiabatic este caracterizat prin aceea că are loc fără schimbul de căldură cu mediul înconjurător. Formula pentru prima lege a termodinamicii se reflectă după cum urmează:
Într-un proces adiabatic de gaze efectuează muncă datorită energiei sale interne.
Exemple de soluții referitoare la sarcini „prima lege a termodinamicii“
Figura 1 prezintă izoterma AB și CD. Ia raportul dintre cantitatea de căldură (), care primește aceeași masă de gaz în procesele I și II. Luați în considerare masa gazului în același proces.
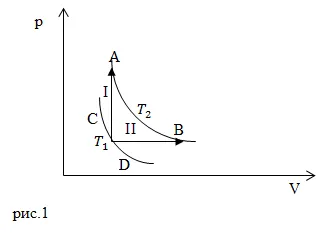
Procedeul I este izocoră. Pentru procesul de izocoră, prima lege a termodinamicii poate fi scris ca:
Procesul II - este izobarice, prima lege a termodinamicii pentru aceasta ia forma:
unde am folosit ecuația de stare a procesului izobară gaz ideal și sunt considerate starea inițială și finală a gazului:
Derulați la raportul dorit:
=
Care este cantitatea de căldură raportată gaz ideal monoatomic în valoare de moli, dacă ar fi cheltuit cu el de încălzire izobară? Schimbarea temperaturii în K.
Baza pentru rezolvarea problemei este prima lege a termodinamicii, care este procesul de izobară poate fi scris ca:
Pentru procesul de izobară a gazului de lucru este egal cu:
Schimbarea în energie internă a procesului nu depinde, precum:
Deoarece procesul este realizat cu un gaz ideal, starea sa poate fi descrisă de ecuația Mendeleeva- Clapeyron:
La o presiune constantă pentru două state au luat in considerare de gaz:
Luând în considerare expresiile (2.3) și (2.5), prima lege a termodinamicii pentru procesul de izobară poate fi scris ca:
în cazul în care pentru un monoatomică număr molecula de gaz de grade de libertate egală.
Se calculează cantitatea necesară de căldură: