Cum de a scrie o formulă structurală, fac totul singur
Formula structurală - este o reprezentare grafică a structurii chimice a moleculelor dintr-o substanță care prezintă ordinea atomilor, dispunerea lor geometrică. În plus, se arată în mod clar valența atomilor elementului constitutiv.
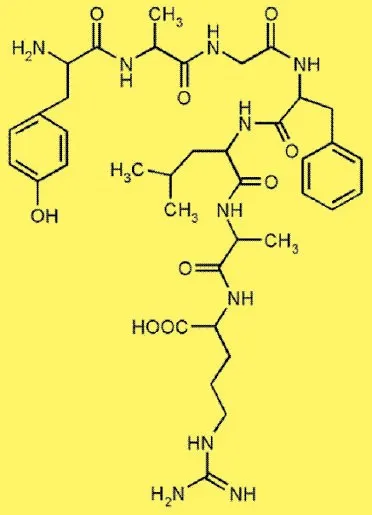
- - mânerul;
- - hârtie;
- - sistemul periodic al elementelor.
instrucție
1. Pentru ortografia corectă a formulei structurale a oricărui alt produs chimic, trebuie să știți foarte bine și imaginați-vă ce capacitatea de atomi pentru a forma un anumit număr de perechi de electroni cu alți atomi. Ceaiul este o valență va ajuta să atragă legături chimice. De exemplu, formula dată NH3 amoniac molecular. Vi se cere să scrie formula structurală. Să considerăm că hidrogenul invariabil monovalent, în consecință, atomii pot fi legate, în consecință, ar fi combinat cu azotul.
2. Pentru a scrie în mod pozitiv formulele structurale ale compușilor organici, se repetă de bază AM aranjament teorie Butlerova prin care există izomeri - o substanță cu aceeași structură de bază, dar cu diferite proprietăți chimice. De exemplu, izobutan și butan. Formula moleculară au identic: C4H10 și structural - sunt diferite.
3. liniar formula întregului atom înregistrate separat, în consecință, o astfel de imagine ocupă mult spațiu. Cu toate acestea, în prepararea formulelor structurale, puteți specifica numărul generală de atomi de hidrogen de la oricare atom de carbon. O egalitate între legături chimice carbon adiacenți sub formă de linii.
4. Izomerii de scriere începe cu o structură tipică a hidrocarburii, adică catena liniară de atomi de carbon. După aceea, se taie la un atom de carbon, unul care atașați la altul, carbonul intern. După epuizarea tuturor izomerilor grafii cu această lungime a lanțului, se taie chiar și un atom de carbon. Din nou, atașați la un lanț de atomi de carbon intern. De exemplu, formula structurală de n-pentan, izopentan, tetrametilmetana. Astfel, o hidrocarbură cu formula moleculară C5H12 are trei izomeri.
Unii pînă acum shudder lecții amintesc chimie, în care a fost necesar pentru a face formula structurală a hidrocarburilor și izomerii acestora. Între timp, nimic despre asta descurajantă. Destul de ghidat în prepararea formulelor pentru anumite algoritm.
instrucție
1. Descopera hidrocarbura formula moleculară. Pornind de la aceasta, să facă o primă formulă schelet de carbon neramificată (lanț de carbon).
2. Deasupra fiecare atom de carbon se înscriu numărul său de serie.
3. Apoi aranjați atomii de hidrogen din catena. Nu uita: de carbon este tetravalent.
4. Reducerea lanțului de carbon cu un atom. Puneți-l ca o ramură laterală a lanțului de carbon. Nu uitați că atomii sunt aranjate la atomii de lanț extreme, nu pot fi ramurile laterale.
5. Se determină la ce margine ramură laterală mai aproape. Numărul de catena de carbon din nou, din moment ce această regiune. Aranjați atomii de hidrogen, în conformitate cu valența de carbon.
6. Determina dacă ramura laterală permisă plasată la alți atomi de carbon în catenă. În cazul unui rezultat corect al formulei compune izomeri. Dacă o astfel de probabilitate este absent, reduce atomul lanțului de carbon primar și o altă poziție ca pe o altă ramură laterală. De notat că lângă un atom de carbon nu este permis să cedeze VIZĂ 2 ramuri laterale.
7. Spread numerele de secvență de atomi de carbon de la margine, care este mai aproape de fiecare ramură laterală este localizată. Poziția aproape toți atomii de hidrogen sunt atomi cu valența de carbon.
8. Din nou, a verifica dacă există probabilitatea ca ramuri laterale poziționate la alți atomi de carbon în lanț tija. Dacă există o astfel de posibilitate, care alcătuiesc izomerii acceptabili formula - în cazul în care nu, scad catena de carbon cu un alt atom, și poziționați-l ca ramură laterală. Acum, în număr întregul lanț de atomi și de a crea formula Reîncercați izomeri. În cazul în care deja două ramuri laterale sunt situate la distanță identice de marginile lanțului, începe numerotarea de la marginea, care ramurile laterale sunt enorme.
9. Continuați să efectuați acești pași, până la epuizarea până când toate probabilitățile localizarea ramurilor laterale.
Pentru a face compoziția chimică și înregistrarea regulilor definite structura chimică pentru prepararea de formule chimice, cu un ajutor de caractere speciale, simboluri au fost făcute, numerele auxiliare și caractere.
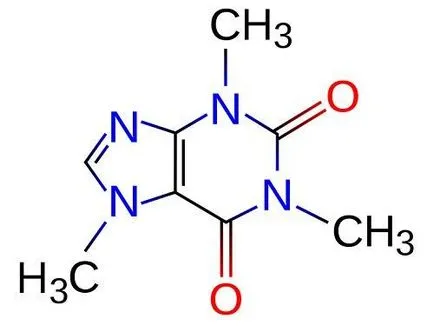
instrucție
1. Formula chimică a ecuațiilor sunt implicate în scrierea de reacții chimice, o reprezentare schematică a proceselor chimice, conexiuni. Pentru scrierea lor se aplică așa-numita limbă de chimie, una care reprezintă un set de simboluri, cum ar fi simbolurile elementelor, numărul de atomi ai fiecărui element în materie descris și așa mai departe.
2. Simbolurile elementelor chimice - una sau mai multe litere ale alfabetului, din care primul titlu. O înregistrare schematică numire full element, de exemplu, Ca - este calciul sau armură. Calciu.
3. Numărul de atomi exprimate prin numere matematice, spun, H_2 - este de doi atomi de hidrogen.
4. Există mai multe metode de înregistrare formula chimică. simplu, empirică, rațională și structurală. Cea mai simplă formulă de înregistrare reprezintă raportul dintre componentele chimice cu masa nucleară, care este specificată ulterior semnul unui element chimic ca subscript. De exemplu, H_2O - formulă simplă a moleculei de apă, adică doi atomi de hidrogen și un atom de oxigen.
5. Formula chimică empirică este diferit de primitiv care reflectă compoziția materialului, dar nu structura moleculară. Formula arată numărul de atomi într-o singură moleculă, care este, de asemenea, descris ca un subscript.
6. Diferența dintre un formule primitive și empirice arată înregistrarea benzenului cu formula: CH și C_6H_6 respectiv. Ie Cea mai simplă formulă prezintă o corelare directă a atomilor de carbon și hidrogen, în timp ce empirică substanța menționată în moleculă conține 6 atomi de carbon și 6 - hidrogen.
7. Formula rezonabilă arată în mod clar prezența grupelor de atomi de elemente din compus. Astfel de grupe sunt date în paranteze, iar numărul lor este indicat de subscriptului după paranteze. Formula se aplică și paranteze pătrate, care sunt complecși ai atomilor (compuși cu moleculă neutră încărcată, ion).
8. Formula structurală este reprezentată grafic în x- sau spațiul 2-dimensional. legături chimice între atomii sunt reprezentate ca linii, atomii sunt specificate de câte ori acestea participă la comun. Mai ales vizual substanța formula exprimă vedere tridimensională, care prezintă un aranjament mutual al atomilor și distanța dintre ele.
Șomajul structural se datorează modificărilor structurale din economie. De multe ori este asociat cu fiecare imbunatatire a procesului de inovare și în diverse domenii ale economiei și agriculturii. Aceste procese nu au susținut multe îmbătrânire de specialitate și de profesie. Ei, în același timp, dau naștere la nevoia de lucrători noi competențe, cel care rămâne nesatisfăcută din cauza lipsei de personal profesionist.

instrucție
1. Șomajul structural, împreună cu frecare este normal. șomaj fricțional este tipic pentru persoanele care tocmai au pierdut locul de muncă și sunt ocupați în căutarea unui nou loc de muncă. Ca de obicei, ea este unul dintre acei experți ale căror profesii sunt încă relevante pe piața muncii. șomaj fricțional se caracterizează printr-o perioadă de scurtă durată de căutare și de așteptare pentru un nou loc de muncă.
2. A doua componentă a obișnuit - șomajul structural, caracterizat printr-o perioadă lungă de timp, de faptul că lucrătorii rămân nereclamate după îmbunătățirea producției, sunt obligate să se supună reconversie și schimbe profesia. Și nu este întotdeauna ușor atât moral și fizic. În plus, acest tip de șomaj se referă la ieșirile și circulația forței de muncă din zonele defavorizate, care afectează, de asemenea, momentul căutării unui nou loc de muncă.
3. Pentru a determina nivelul șomajului structural. trebuie să luați statistici privind șomerilor și să le analizeze. Din numărul general al populației active angajate în căutare de locuri de muncă, aveți nevoie pentru a alege cele de design extrem de profesional, care nu corespunde structurii posturilor vacante existente pe piața forței de muncă. În special, acest tip de șomaj caracterizează experții militari apte de muncă care au rămas nerevendicată în legătură cu reducerea forțelor armate. Ei au adus să se recalifice și să dobândească altele noi, „pașnică“ de specialitate. Se determină numărul de solicitanți de locuri de muncă ale căror cazuri sunt special șomajului structural.
Acorde o atenție!
În cazul în care economia este caracterizată prin prezența a numai șomaj fricțional și structural, acest lucru înseamnă că forța de muncă cu normă întreagă, este deosebit de eficient și de aplicare rezonabilă.
Hidrocarbura - este o substanță organică, care conține numai două elemente de carbon și hidrogen. Poate fi limitative, nesaturate cu dublă sau triplă legătură, ciclice și aromatice.

instrucție
1. Imaginați-vă că aveți următoarele date: densitatea hidrocarburilor la hidrogen - 21, procentul masic de hidrogen este de 14,3%, procentul masic de carbon este de 85,7%. Se determină formula de hidrocarburi.
2. detectează masa molară a substanței pe baza densității sale în raport cu hidrogenul. Rețineți că molecula de hidrogen este format din 2 atomi. Astfel, veți obține 21 * 2 = 42 g / mol.
3. Apoi calcula fracțiunea de masă a carbonului și a hidrogenului în masa molară. * 0,857 = 42 35.994 g - carbon, * 0143 = 42 6,006 g - hidrogen. Rotunjiri aceste valori obține: 36 g și 6 g În consecință, într-o moleculă de substanță conținută 36/12 = 3 atomi de carbon și 6/1 = 6 atomi de hidrogen. Constituenții Formula: C3H6 - propilenă (propenă), hidrocarburi nesaturate.
4. Sau vi se următoarele date: în oxidarea, adică din arderea unui gaz de hidrocarburi. Densitatea de vapori care aerul este 0,552, a fost format 10 g de dioxid de carbon și 8,19 g de vapori de apă. Doriți să afișați formula sa moleculară.
5. Notați ecuația universală de oxidare a hidrocarburilor. SnNm + O2 = CO2 + H2O.
6. molar hidrocarbură masă 0,552 * 29 = 16.008 g / mol. De fapt, cu cât mai aproape de pe această problemă, au fost lăsate să fie considerat rezolvat, prin faptul că se pare că numai o satisface hidrocarburi, această condiție - metan, CH4. Dar aduce o soluție la sfârșitul anului:
7. 10 de grame de dioxid de carbon conținut 10 * 12/44 = 2,73 g de carbon. În consecință, același număr de carbon conținut în hidrocarbura inițială. La 8,19 grame de vapori de apă conținută 8.19 * 2/18 = 0,91 g de hidrogen. În consecință, același număr de hidrogen a fost în materialul inițial. O masă generală de hidrocarbură este: 2,73 + 0,91 = 3,64 g
8. Se calculează procentul de greutate a componentelor: 2,73 / 3,64 = 0,75 pentru un atom de carbon de 75%, 0,91 / 3,64 = 0,25 sau 25% hidrogen. Vezi încă o dată că aceste condiții sunt îndeplinite de o singură substanță - metan. Problema este rezolvată.
sfat sănătos
Pentru a determina valența atomilor în prepararea formulelor structurale folosind sistemul periodic. Arată distanța reală a atomilor din moleculă ajută formula structurală tridimensională.