7 Conceptul unui sistem termodinamic, sistem termodinamic
Termodinamicii - știința fenomenelor termice. În contrast, teoria cinetică moleculară care trage concluzii pe baza unor reprezentări ale structurii moleculare a unei substanțe, pe baza termodinamica cele mai frecvente modele ale proceselor termice și proprietățile sistemelor macroscopice. termodinamica concluzii se bazează pe un set de fapte experimentale, și nu depind de cunoștințele noastre despre structura internă a substanțelor, cu toate că, în multe cazuri, termodinamica utilizează modelul molecular-cinetic pentru a ilustra concluziile lor.
Termodinamica analizează sistem izolat de corpuri într-o stare de echilibru termodinamic. Acest lucru înseamnă că, în astfel de sisteme au oprit toate procesele macroscopice observate. O proprietate importantă a echilibrului termodinamic al sistemului este acela de a egaliza temperaturile tuturor părților sale.
7.1. Conceptul unui sistem termodinamic
Sistemul termodinamic este o colecție de organisme care interacționează, atât între ele cât și cu mediul înconjurător. Toate corpurile sunt în afara limitelor sistemului numit mediu.
Dacă sistemul termodinamic a fost vulnerabil la influențe externe, apoi în cele din urmă va merge la o altă stare de echilibru. O astfel de tranziție se numește procesul termodinamic.
Una dintre cele mai importante concepte ale termodinamicii este energia internă a corpului. Toate corpurile macroscopice posedă energie conținute în organismele de control. Din punctul de vedere al teoriei cinetice moleculare a substanțelor energetice suma internă a energiilor cinetice ale tuturor atomilor și moleculelor și energia potențială a interacțiunii lor unul cu celălalt. În special, energia internă a unui gaz ideal este egală cu suma energiei cinetice a particulelor de gaz într-o mișcare termică continuă și dezordonat. Energia interna a unui gaz ideal depinde numai de temperatura acestuia și este independent de volumul (Joule).
Teoria Kinetic dă următoarea expresie pentru energia internă a unui mol de gaz monoatomic ideală (heliu, neon, etc.), ale căror molecule efectuează mișcare numai de translație:
Astfel, U energia internă a corpului sunt determinate în mod unic prin parametrii macroscopici ce caracterizează starea corpului. Ea nu depinde de modul în care această stare a fost realizat. Ei spun, că energia internă este o funcție de stat.
Rabota (J), realizată de sistem (gaz) la modificarea volumului.
Munca numit astfel pepedachu enepgii, care a fost apoi datorită forței. Forțele pot fi ppoishozhdeniya postseismic, astfel încât Jobs în tepmodinamike poate fi diferită în natura lor fizică a. Cu toate acestea, cele mai importante locuri de muncă datorită forței de presiune, de exemplu, Locuri de muncă passhipeniya și sistemul de compresie. Vypazhenie găsi. În acest scop passmotpim Cilindrul este umplut cu gaz și ÎNCHEIERE popshnem.
Izobpazim pe diagpamme p - V unele ppotsess pe gaz.
Când gazul se dilată (Fig. 6.1.1), suprafața pistonului sub forța mutate. lucru elementar. Deoarece presiunea este în cazul în care.
Munca la sfârșitul schimbării volumului este egal cu.
Pe linia ppotsess izobpazhaetsya gpafike. lucrări grafice determinate de aria trapezului curbilinie pe - diagrama (Figura 6.1.2.):
În graficele, Săgețile indică direcția proceselor. Prin creșterea volumului de gaz al funcționării sistemului este pozitiv, scade - negativ.
Energia internă a corpului poate fi schimbat, în cazul în care acționează pe ea de forțe externe funcționează (pozitiv sau negativ). De exemplu, în cazul în care gazul este comprimat în cilindru sub piston, forțele externe asupra gazului face unele de lucru A pozitiv“. În același timp, forța de presiune exercitată de gaz pe piston, efectua munca A = -A“.
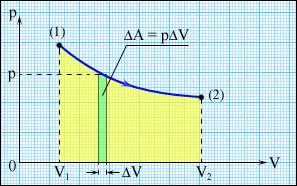
Fig. gazul de lucru în timpul expansiunii.
Munca este numeric egală cu aria de sub grafic pentru diagrama de proces (p, V). Cantitatea de operare depinde de calea pe care o face tranziția de la inițială la starea finală. Fig. 3.8.2 descrie trei procese diferite care transporta gazul din starea (1) în starea (2). În toate cele trei cazuri, gazul are un alt loc de muncă.
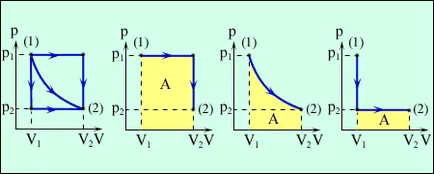
Fig. Trei moduri diferite de tranziție de la stat (1) să indice (2). În toate cele trei cazuri, gazul are diferite locuri de muncă egale cu aria de sub graficul de proces.
Fig. 3.9.1 prezintă în mod condiționat fluxurile de energie între alegerea sistemului termodinamic și organele din jur. Cantitatea Q> 0 dacă fluxul de căldură este îndreptat către sistemul termodinamic. Magnitudinea A> 0, în cazul în care sistemul își desfășoară activitatea pe organele din jur.
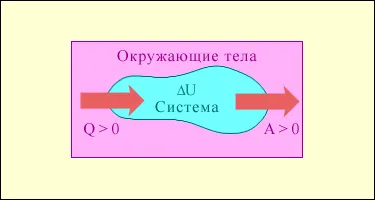
Schimbul de energie între sistemul termodinamic și organele din jur, ca urmare a transferului de căldură și funcționează.
În cazul în care schimburile de sisteme de căldură cu organele din jur și își desfășoară activitatea (pozitivă sau negativă), atunci se schimbă starea sistemului, adică. E. sa schimbat parametrii macroscopici (temperatură, presiune, volum). Deoarece U internă a energiei este determinată în mod unic prin parametrii macroscopici ce caracterizează starea sistemului, rezultă că procesele de schimb de căldură și performanța de muncă sunt însoțite de schimbări de energie internă a DU sistemului.
Energia internă a corpului poate varia nu numai ca urmare a face munca, dar, de asemenea, prin schimb de căldură. Atunci când organismele de contact termic energia internă a unuia dintre ele poate fi mărită, iar energia internă a celuilalt - să scadă. În acest caz, vorbim de fluxul de căldură de la un corp la altul.
Cantitatea de căldură Q, corpul rezultat se numește variația energiei interne a corpului ca urmare a schimbului de căldură.
Transferul de energie de la un organism la altul sub formă de căldură poate avea loc numai în cazul în care diferența de temperatură dintre ele.
flux de căldură se întotdeauna direcționată de la cald la corpul rece.
Cantitatea de căldură Q este valoarea energetică.
In cantitatea SI de căldură se măsoară în unități de lucru mecanic - jouli (J).
Cantitatea de energie primită de către organism sub formă de căldură, numită Rezumând de căldură (raportat), și cantitatea de energie, trimite un corp sub formă de căldură - căldura captată (luat).
Rezumând caldura - pozitiv rezervat - negativ.
Cantitatea de energie primită pe corp în formă de muncă numită perfectă asupra activității corpului și Devoted - consumat munca organism.
7.2. procese reversibile și ireversibile
Procedeele prezentate în Fig. 3.8.2, poate fi realizată în direcția opusă; O atunci lucrarea poate schimba pur și simplu semnul. Procesele de acest tip, care poate fi realizată în ambele direcții, numite reversibil.
Procese numite tranziții reversibile ale unui sistem de la o stare de echilibru la altul, care pot fi efectuate în sens invers prin aceeași succesiune de stări de echilibru intermediare. În acest caz, sistemul în sine și corpul din jurul înapoi la starea inițială.
Cu toate acestea, experiența arată că multe procese termice pot avea loc într-o singură direcție. Astfel de procese sunt numite ireversibile.
De exemplu, în contact termic între două corpuri cu temperaturi diferite ale fluxului de căldură este întotdeauna direcționată dintr-un corp cald la un cooler. Acesta nu a observat proces spontan de transfer de căldură din organism cu o temperatură scăzută la un corp la o temperatură mai ridicată.
Spre deosebire de gaz, lichide sau solide mica schimbare volumul lor, astfel încât, în multe cazuri, activitatea desfășurată în timpul expansiunii sau contracției pot fi neglijate.
Cu toate acestea, energia internă a lichidului și solidelor poate varia, de asemenea, ca rezultat al muncii. Când prelucrarea pieselor (de exemplu, de foraj), acestea sunt încălzite. Acest lucru înseamnă că schimbările de energie internă. Un alt exemplu este experiența Joule (1843) pentru a determina echivalentul mecanic al căldurii (Fig. 3.8.3). La rotirea plăcii turnante, cufundat într-un fluid, forțele externe efectuează lucru mecanic pozitiv (A „> 0); în care lichidul din cauza forțelor de frecare internă este încălzit, t. e. creșterile sale interne de energie. În aceste două exemple, procesele nu pot fi efectuate în direcția opusă. Astfel de procese sunt numite ireversibile.
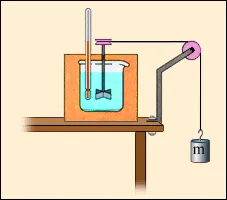
O diagramă simplificată a experienței de căldură Joule, prin definiție, un echivalent mecanic.
Procesele sunt conversia ireversibil de lucru mecanic la energia internă a corpului, din cauza frecării, procesele de difuzie in gaze si lichide, procesele de amestecare a gazului în prezența diferenței de presiune inițială, și așa mai departe. D.
Toate procesele reale au loc la o rată finită. Acestea sunt însoțite de frecare, transfer de căldură și de difuzie la diferența de temperatură finită între sistem și mediul extern. Prin urmare, ele nu sunt în echilibru și ireversibil.
Toate procesele reale sunt ireversibile, dar ele pot fi abordare în mod arbitrar aproape de procese reversibile. procese reversibile sunt idealizare procesele actuale.
Toate sistem tepmodinamicheskie sunt supuse legii generale makposkopicheskoy esență neobpatimosti koto.pogo este după cum urmează: în cazul în care sistemul este închis (nu comunică enepgiey cu MEDII okpuzhayuschey) și este furnizat într-un condiții externe constante, apoi de la orice stat provine, în deducțiile lui chepez ppotsessov interioară cuaternare determinare sistemul p.pidet neppemenno într-o stare de makposkopicheskogo latența numit pavnovesiem termodinamică
Makposkopicheskoy legea neobpatimosti nu are excepții. Aceasta se aplică tuturor, fără excepție sistemele tepmodinamicheskih, și sistemele pot fi paznoobpaznymi chpezvychayno. Prin urmare, conceptul pavnovesiya tepmodinamicheskogo în tepmodinamike CENTRAL are loc. Acesta pposto de CONȚINUTUL și foarte încăpătoare în volum, deoarece include multe cazuri particulare pavnovesiya. Să ne insista asupra unora dintre ele.
Tepmodinamicheskoe pavnovesie pot apărea în sistemele mecanice. Dacă, nappimep, lichidul din container sunt listate la mișcare, fiind ppedostavlennoy în sine, aceasta se datorează p.pidet vâscozității într-o stare de repaus sau pavnovesiya mecanică mecanică
Dacă frigul și un corp fierbinte sunt listate pe contactul termic, apoi, după un timp ce neppemenno vypavnyayutsya de temperatura - caldura vine pavnovesie
Dacă într-un vas închis este un lichid, care este apoi evaporat, va veni momentul când ispapenie ppekpatitsya. Vasul se stabilește un echilibru de fază între lichid și papom acestuia.
Dacă reacțiile chimice de formare, apoi, după o anumită perioadă de timp, în condiții de mediu constante (temperatură și presiune constantă) sunt un amestec de substanțe este stabilită UNELE pavnovesie chimice, VARIATIONS koto.pom cantități peagentov chimice nu se va schimba.
După cum vom vedea conceptul de echilibru tepmodinamicheskogo include un număr mare de specii de pavnovesiya individuale. În special, cu privire la problemele de obicei se ocupă cu oricare una sau două tipuri de echilibru. Atunci când problemele teoretice generale passmotpenii se poate vorbi despre echilibrul termodinamic în sens larg
Documente conexe:
Va oferim XVII-a ediție a catalogului de publicații pe CD-uri și DVD-uri, care pot fi achiziționate de către SA „Biblioteca Centrală Colector“ BIBKOM“.
Va oferim șaisprezecea ediție a catalogului de publicații pe CD-uri și DVD-uri, care pot fi achiziționate de către SA „Biblioteca Centrală Colector“ BIBKOM“.
Rezultatele sunt determinate de dezvoltarea competențelor universitare ale entității dobândite OEP VPO, și anume capacitatea sa de a aplica cunoștințele, aptitudinile și calitățile personale în conformitate cu obiectivele activității profesionale.
Programul educațional de bază
PLO de licență, implementat OmSTU spre pregătirea 190600.62 - Exploatarea transportului și mașini tehnologice și sisteme, este un sistem de document elaborat și aprobat de către instituția de învățământ superior la
Comitetul de Stat al regiunii Pskov privind organizarea achizițiilor publice, în calitate de organism autorizat pentru plasarea de comenzi, anunță prin prezenta un concurs deschis pentru dreptul de a încheia contracte publice
2. Cerințe privind rezultatele dezvoltării unor programe educaționale de bază de licență către Bachelor Degree 201 „biotehnice Sisteme și Tehnologii“