Procentul molar - Referință chimistului 21
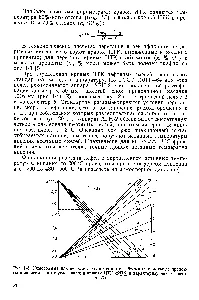
Fig. 1-3. Un nomograma pentru conversia fracțiunii distilate în vrac, în procente molare, în funcție de unghiul de înclinare a curbelor și mk CTI și factorul care caracterizează (K).
Fracția molară este de asemenea numit un molar sau molecular, narcotizant sau fracție. Este egal cu 100 procente molare Ni. [C.296]
Concentrația, exprimată în procente molare (j%), este raportul dintre numărul de moli de rij component / mol la tii suma tuturor componentelor amestecului, înmulțit cu 100 [c.103]
Recalcularea concentrare solute. exprimată în grame echivalenți per 1 litru de soluție (Sd), în procente molare - concentrație, exprimate în gram-molecule ale substanței per 100 g mol soluție (W), se poate face prin formula [C13]
EXEMPLU EXEMPLU Se calculează gradul de echilibru de conversie de azot și hidrogen în amoniac la o temperatură de 427 ° C și o presiune de 300 atm. Compoziția inițială a gazului în azot procente molare de 25%, 757o hidrogen. Reacția are loc conform ecuației [C.18]
După cum se vede din tabel, solubilitatea așa-numitele gaze permanente (hj, N2, CO, O2) este mică (câteva sutimi și câteva zecimi de procent prin mol). Relativ ridicată solubilitatea etilenei, dioxid de carbon, clor, datorită faptului că temperaturile critice ale acestor gaze sunt ridicate și aproape de temperatura critică a solventului. decât aceeași valoare pentru gazele permanente. [C.225]
Mai convenabil pentru a identifica modele în proprietățile soluțiilor nu este o cantitate în greutate comparație componentelor. și cantitățile molare. în care, în acest caz, compoziția poate fi exprimată în fracții molare. și procentul molar. [C.295]
Mole procente - numărul de moli de substanță dizolvată în 100 g soluție-mol. [C.12]
K - procentul molar de combustibil nears în produsele de ardere. [C.10]
CO2, O2 - procentul molar al substanțelor individuale în combustibili [c.54]
Utilizarea nomograma este ilustrată prin exemplul prezentat în Fig. 22 este necesară pentru a determina cât de multe procente molare corespund la 30% (în greutate). Benzen în amestec benzen toluen. Este cunoscut faptul că pentru benzen = 78,11, și toluen pentru M = 92.13. Apoi 78.11 / 92.13 = 0,848 0,85. [C.37]
procentul molar H de combustibil nears din gazele de ardere. [C.54]
Compoziția amestecului exprimă întotdeauna concentrația de component volatil. în cazul în care nu este specificat în mod special. Concentrarea indicată în volum, greutate sau fracții molare sau în cea mai mare parte, masa sau procent molar. [C.34]
Dacă luăm în considerare liniile orizontale I și II pe RNS. 43, pentru care pe abscisă diagramele indicate concentrație în procente molare bazat pe componenta extrem de volatilă (vezi. De asemenea, fig. 29), următoarele relații pot fi identificate. [C.72]
Triunghiulare diagrama. Compozițiile amestecurilor reprezentate folosind Gibbs nodurile triunghi caracterizează componentele pure sale A, B și 5 și reprezentate grafic pe laturile greutății (uneori mol) procente. Fig. XI1-1 diagrame triunghiulare prezentate cele mai frecvente tipuri de amestecuri ternare 1 [c.388]
Care formează procente molare-alchene hidrocarburi aromatice ing a izopropilbenzen la următoarele reacții la 1000 ° K și 1 atm, dacă 1 mol de cumen este luată pentru reacția [c.215]
Dacă ciclopentan și derivații săi nu sunt pre merizovat în structura izo-St-ring, apoi dehidrogenarea ei nu formează o hidrocarbură aromatică [256, 257]. Întrucât condițiile termodinamice la temperaturi de peste 300 ° C, sunt favorabile pentru formarea hidrocarburilor aromatice [258], în timpul prelucrării termice de compuși aromatici ciclohexanului nu se formează. La o temperatură de 550 ° C a produs cantități foarte mici de benzen, [259], iar la 620 ° C, randamentul de compuși aromatici este de numai 0,4 procente molare, în ciuda faptului că descompunerea suferă o cracare% ciclohexan 24 [260]. derivati Partial alchil ai ciclohexil [c.101]
Condensarea acetonă poate fi obținut izoforon. utilizat ca solvent. În ceea ce privește procentul molar de randamentul teoretic va varia. dacă nu iau în considerare faptul că starea de sistem imperfect. Reacția se efectuează RCT 500 ° K și 35 atm cu 3 moli de acetonă [c.219]
In cele de mai sus (p. 485 ff.) Calcularea numărului de talere teoretice prin y-diagrama permit căldurilor molare egale de evaporarea componentelor și cantitatea ulterioară a constanței lichidului și a vaporilor în înălțime coloana de distilare. In a fost observat pentru ca această ipoteză, materialul trebuie să se efectueze calcule, exprimând toate valorile sau de la kmol procente molare, din cauza necesității de a recalcula unitățile de ponderare pe mol. În plus, atunci când se calculează în conformitate cu diagrama x-y nu sunt capturate căldură. livrat cu sau pierdute prin distilare. [C.502]
Presiunea, kg / cl 2 procente mol de metan în smesn [c.97]
Rezultate satisfăcătoare pot fi obținute pentru sistemele care conțin mici cantități de azot și dioxid de carbon [4, 5, 6, 28, 29], atunci când este aplicat la greutatea moleculară reală a azotului și a dioxidului de carbon. Fig. 22 ilustrează un acord între valorile primite și calculate ale constantelor de echilibru pentru metan în cele trei sisteme ternare. conținând 5 moli la sută azot la temperatura de 26,7 ° C. Punctele indică datele experimentale pe curbele de echilibru - valori. calculată din graficele, baza pentru construirea de care este prevăzut sistemul de parafină. Deviația maximă dintre constantele de echilibru calculate și cele observate pentru metan, în acest caz [4, 5, 6] egal cu 5%. [C.111]
fracție molară poate fi exprimată în fracțiuni de unitate, și ca procent (în acest ultim caz, se numește procentul molar). [C.179]
Kontsengratsiya în fracțiuni molare determinate numai de compoziția și faza nu este dependentă de temperatură și presiune. Dacă valoarea sa este înmulțită cu 100 pentru a obține concentrația componentei în procente molare (mol ° / o). [C.207]
Temperatura de cristalizare comparativ. compoziția amestecului este de asemenea exprimat grafic. În acest scop, axa abscisă reprezintă compoziția în greutate sau procente molare, iar temperatura de topire a axei y (cristalizare). Un astfel de grafic se numește fuzibilitate diagramă. [C.41]
Bhutan. n-Butanizomerizuetsyav YuOraz mai repede decât izobutap [422]. În fază lichidă, cu adaos de 5 procente molare de catalizator (bromură de aluminiu) la 27 ° C sub o presiune de 3 amestec echilibrat kPsm de n-butan și izobutan conține aproximativ 78- 82% din aceasta din urmă. Necesar de 1000 de ore pentru a ajunge la această condiție, nici alte produse sunt formate, iar catalizatorul rămâne neschimbat [411, 423, 424]. Viteza de reacție depinde de concentrația de temperatură și catalizator. La temperaturi ridicate sunt reacția redistribuție vizibile. [C.117]
reacție Redistribuirea atașate legături duble în toate cazurile sunt generate cu ușurință mai mari sau produse substituită cu alchil inferior. De exemplu, xileni suferi redistribuire în prezență de acid fluorhidric. trifluorura de bor sau clorura de aluminiu [501] pentru a forma un benzen, toluen și produse de alchilare superioare. Selectarea corectă a condițiilor de redistribuire poate fi realizată cantitativ. Astfel, în prezența a 90 moli trifluorura de bor procente etilbenzen formează un amestec de benzen și [c.126]
Dintr-un teren de Urad din Hv (Fig. 61), se poate vedea cu ușurință că, în concentrația componentului de fierbere scăzut sub 10% (mol.) Reducerea concentrației sale per procent molar necesită o creștere semnificativă a numărului oroshayush, acesta fluid. În practică, distilarea este inițiată de obicei, la un raport de reflux de n = 2, iar temperatura este ridicată la partea superioară a coloanei [c.102]
oxigenați de izomerizare. În 1963-1965. Henkel (Germania), a dezvoltat un procedeu de obținere a acidului tereftalic de săruri de potasiu de înaltă puritate ftalic sau acid izoftalic. Schema procesului prezentat în Fig. 3.16. Uscate în aparat I sare de potasiu. care nu conține apă de cristalizare. Se trece prin reactorul 2 în atmosferă Oj, la 400-430 ° C sub o presiune de 0,5-2,0 MPa, în prezența unui catalizator sub formă de particule de cadmiu. luate într-o cantitate de câteva procente molare. În aceste condiții, gradul de conversie a materiei prime este de aproape 100% randament dikaliytereftalata ajunge la 95-98%. [C.94]
Exemplu. Soluția conține 1000 g apă 100 g de KNO3, 200 g și 150 g Nanog KC1. Se determină compoziția soluției a) săruri de molecule gram per 1000 g mol de apă, b) în procente molare, c) la procentaj echivalent și g) în procente ion echivalent. [C.18]
În ecuația (VI-16) nu este inclus vapori de peidealnost și faze lichide, astfel încât presiunea să fie redusă, iar solubilitatea mică, în majoritatea cazurilor mai puțin de un procent molar. Spre deosebire de coeficienții Bunsen în calculul coeficienților Ostwald și volumul de gaz este luată la o temperatură a sistemului. Astfel, și prin înlocuirea în ecuația (VI-16), trebuie remarcat faptul că [c.81]
Presiunea, kg / SL12 Procentul molar de metan în amestec [c.97]
U 20 30 40 50 60 70 80 90 100 Procentul molar de azot din dzaze lichid [c.98]