Procedura de înregistrare de stat a BAS în Rusia
Ne pare rău, dar browser-ul dvs. nu acceptă redarea fișierului audio. Încercați un alt browser
Ne pare rău, dar browser-ul dvs. nu acceptă redarea fișierului audio. Încercați un alt browser
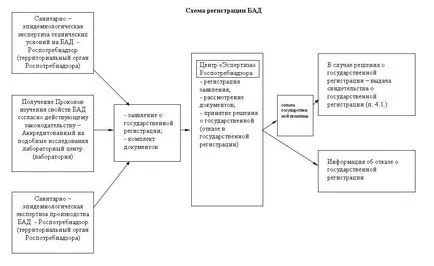
Procedura de înregistrare de stat BAD
în România
Luați în considerare procedurile persoanei juridice (producător sau vânzător), a luat decizia de a produce și / sau de aprovizionare a pieței cu aditivi biologic active (în continuare - BAS).
Trebuie remarcat, la o dată că nici o organizație autorizată să efectueze vânzarea cu amănuntul de suplimente alimentare (în conformitate cu alin. 7.4. SanPiN 2.3.2.1290-03. Suplimente de vânzare cu amănuntul prin intermediul farmaciilor (farmacii, magazine farmacie, farmacie, etc.), sau magazine de specialitate pentru vânzarea de produse alimentare de sănătate, magazine alimentare (departamente speciale, secțiuni, chioșcuri), nu iau suplimente, fără realizarea documentelor de autorizare relevante, și anume:
- certificatul de înregistrare de stat pe teritoriul România;
- certificat de calitate pentru baa de la producător.
Primul document cu care se confruntă producătorul - este SanPiN 2.3.2.1290 - 03 „cerințele de igienă ale producției și cifra de afaceri de aditivi biologic active (BAD)“. Acesta definește un număr de evidențiază, pune bazele pentru soarta în continuare de suplimente alimentare, și anume:
- Cerințe pentru producerea baa documentației tehnice (razdelIIISanPiN 2.3.2.1290 - 03). Merită să rămână și pentru a sublinia faptul că nu puteți lua de acid citric și de zahăr, se amestecă și se înregistra ca un supliment alimentar. Un astfel de produs va fi oprit la stadiul examinării documentației tehnice: specificațiile tehnice (TU) și instruirea tehnologică (TI);
- cerințele de ambalare și completează informațiile imprimate pe etichete (razdelIVSanPiN 2.3.2.1290 - 03). Atunci când se aplică pentru ambalaje de consum de examinare baa trebuie să fie prevăzută cu un decal pe care informațiile sunt reglementate de legislația aplicată în viitor, în cazul în care baa va găzdui succes înregistrarea, producătorul va fi necesar să se aplice la fiecare număr de etichetă certificatului de înregistrare de stat și data emiterii acesteia;
- Sanitare - cerințe epidemiologice pentru producerea de suplimente alimentare. Acest articol se referă în primul rând la producător. Fără a obține sanitare - epidemiologice concluzie, în care autoritatea teritorială Rospotrebnadzor (Anexa 2 la numărul de reglementări administrative) va da o evaluare pozitivă a condițiilor (cu alte cuvinte, le numesc „relevante“), producția și înregistrarea suplimentelor alimentare nu sunt posibile.
Astfel, producătorul a elaborat caietul de sarcini, TI a dezvoltat și fabricat format de etichetă, a primit sanitare - certificat epidemiologic pentru producție.
Acum, el poate trece la următoarea etapă de înmatriculare BAD: BAD fabricarea lot, pachet l într-un ambalaj de consum SanPiN2.3.2.1290 corespunzător - 03. lipi etichete în conformitate cu același document normativ și să înceapă procesul de înregistrare.
Autoritatea de înregistrare ( „Expertiza“ centru Rospotrebnadzor www.crc.ru) următoarele documente (anexa 5 la numărul de reglementări administrative):
- Declarația întocmită în conformitate cu anexa 4 la normele administrative - TU, reteta SUT pentru suplimente, care ar trebui să efectueze de fabricație industrială a produselor certificate în conformitate cu legislația România;
- Daca TU si TI Numarul trecut deja înainte de examinare, trebuie să furnizeze sanitar - epidemiologică pentru confirmare, certificată în conformitate cu legislația România;
- Sanitare - certificat epidemiologică a respectării condițiilor de cerințele de producție ale normelor sanitare-epidemiologice de stat și norme, certificate în conformitate cu legislația România;
- instrucțiuni de utilizare (se introduce pachetul, abstract) (în cazul în care toate informațiile necesare nu pot fi introduse pe etichetă), certificate de semnătură autorizată și ștampila producătorului;
- consumator (sau tara), o etichetă sau un proiect de certificat prin semnătură autorizată și ștampila producătorului;
- rapoarte de testare a laboratoarelor de testare acreditate (centre), concluziile organizațiilor acreditate (organoleptice, fizico-chimice, microbiologice, investigatii radiologice (teste), studierea conținutului permis chimice, componente radiologice, biologice, interzise și compușii acestora, microorganismele și alți agenți biologici reprezentând pericol pentru sănătatea umană, în conformitate cu sanitar de stat și a normelor și reglementărilor epidemiologice);
- actul de prelevare a probelor (eșantionare) formă fixă - cu o marcă comercială - o copie a unei mărci comerciale, certificată în mod corespunzător
- cazul în care producătorul și solicitantul sunt diferite persoane juridice (fie de către producător trebuie să prezinte organismului de înregistrare o persoană), la cerere și un set de documente solicitate avocat producătorului că el are încredere reclamanta să le reprezinte interesele pe teritoriul România pentru punerea în aplicare a înregistrării de stat a produselor producătorului precum și puterea de avocat pentru dreptul de a obține un certificat de înregistrare de stat a suplimentelor alimentare.
Revenind un pic înapoi, observăm că în mâinile ne-au toate documentele din listă, cu o singură excepție: raportul de încercare al centrului de testare acreditat (de laborator).
Expertiza (expertiza sanitară și epidemiologică, precum și de cercetare, de testare, toxicologice, igienice și de alte tipuri de evaluări), necesare pentru înregistrarea de stat se exercită de către agențiile guvernamentale federale - igiena si centre de epidemiologie (lista de facilități disponibile pe site-ul internet oficial al Serviciului federal de supraveghere în domeniul protecției drepturilor consumatorilor și bunăstarea umană: www.rospotrebnadzor.ru), alte organizații, acreditate în conformitate cu procedura stabilită (lista organizațiilor publicat pentru prima dată pe site-ul oficial al Agenției Federale pentru Reglementare tehnică și Metrologie: www.gost.ru).
Ciuma „Centrul federal de igienă și epidemiologie“ al Rospotrebnadzor.
«Centrul de Igienă și Epidemiologie din Moscova“ Rospotrebnadzor.
Institutul de Cercetare de Medicina Muncii de Stiinte Medicale (de acord).
Institutul de Cercetare de Ecologie Umana si Igiena Mediului le. AN Stiinte Sysina (prin acord).
Federal Centrul de Cercetare al acestora Igiena. F.F.Erismana Rospotrebnadzor.
Institutul de Cercetare de Nutriție (care urmează să fie convenite).
Institutul de Cercetare de igiena si de ingrijire a sanatatii pentru copii și adolescenți de Stiinte Medicale (de acord).
Institutul de Medicină Fizică și chimice (în acord).
Academia Română Medicală Postuniversitare Educație University Medical (așa cum a fost de acord).
FSIS „Institutul de Cercetări București, de Igiena Radiațiilor dupa profesorul PV Ramzaev „Rospotrebnadzor.
Desigur, acest lucru nu neagă dreptul de a aplica pentru raportul de încercare al producătorului în orice alt acreditat pentru o astfel de centru de cercetare sau de laborator, cu toate acestea, sunt specificate în lista centrelor de laborator sunt legitime și a emis rapoartele lor vor fi luate cu siguranță statul autorității de înmatriculare BAA.
Procedura de înregistrare este finalizată.
1. reglementări administrative
Rospotrebnadzor
Performanța funcțiilor publice cu privire la înregistrarea de stat introdus pentru prima oară în producție, în trecut, să nu folosească substanțe chimice și biologice și fabricate pe baza acestora, potențial pericol pentru om (altele decât DROGURI); Produsele particulare prezintă un pericol potențial pentru om (altele decât DRUGS); Anumite tipuri de produse inclusiv alimente, LA IMPORTATE PRIMA ZONĂ România (documentul MS Word 404 KB)
2. SanPiN 2.3.2.1078-01.doc (document MS Word 3448 KB).
3. SanPiN 2.3.2.1290-03.doc (document MS Word 249 KB).