Prezentarea pe bază seria Omologii concepte de hibridizare omoloage radicalilor liberi
Prezentarea intitulat „Concepte de hibridizare omoloagă din seria radicalilor liberi omologi izomerism, izomeri capacitatea de a distinge principal izomeri ai componentei omologi.“ - Transcrierea:
1 Concepte hibridizare seria omoloagă Radicalii liberi omologi izomerie izomeri capacitatea principal de a distinge izomerii Omologii Compile formula structurală

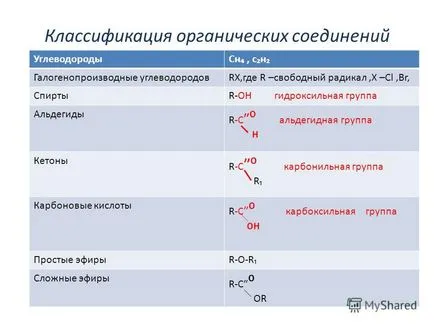
2 Clasificarea compușilor organici UglevodorodySn cN halogenati uglevodorodovRX, în care R este un radical liber, X este -CI, Br, SpirtyR-OH gruparea hidroxil de aldehide R-C grupare aldehidă grupare Cetone R-C carbonil R acizilor carboxilici R-C grupă carboxi Simple efiryR-esteri ai R-C OR
3 hidrocarburi C n H 2 n + 2 limită C n H 2 n cicloparafine, etilenic C n H 2 n 2 diene, acetilenic C n H 2 n aromatic 6

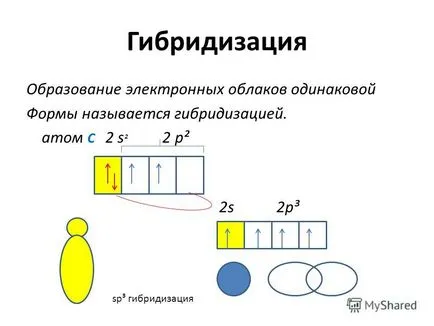
4 Hibridizarea Educația norilor de electroni aceeași formă se numește hibridizare. atomul C 2 s ² 2 p² 2s 2p³ sp³ hibridizare
5 hidrocarburi saturate C n H 2 n + 2 cicloparafine C n H 2 n sp² hibridare etilenică C n H 2 n, diene C n H 2 n 2, aromatic C n H 2 n 6 sp hibridare aceîilenic C n H 2 n- 2

6 atomi de C Ϭ legătură sigma Ϭ sigma legătură Ϭ sigma legătură π π 2 pi legătură pi legătură simplă legătură de carbon din cauza orbitali hibridizate numit Ϭ sp³ sp² sp

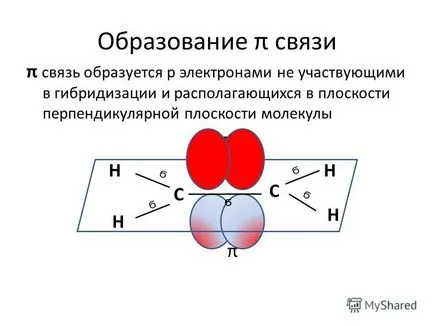
7 Educație π comunicații H H H H C C Ϭ Ϭ Ϭ Ϭ Ϭ π legătură este format p electroni nu participă la hibridizare, și aranjate într-un plan perpendicular pe planul moleculei tt π
8 seria omoloagă C n H 2 n + 2 CH - metan CH - hexan CH - etan CH - CH heptan - propan CH - octane CH - -butan CH - nonan CH - pentan CH - Omologii decan - o substanță similară în structură și proprietăți și care diferă unul de altul prin una sau mai multe grupări CH

particule 9 Radicalii liberi activi având un electron liber este numit un radical liber. NH Ñ: S̤ϞN = H: M · + H · H H CH = CH · + H

10 Radicalii liberi CH - CH metil - CH hexil - etil CH - CH heptil - propil CH - CH octil - butii CH - CH nonil - pentil CH - dekil două grupuri - di; Trei sau trei; Patru - tetra; Cinci radicali -penta totală formula C n H n +
11 Fenomenul izomerie constă în existența unor conexiuni multiple cu aceeași compoziție cantitativă și calitativă cu aceeași greutate moleculară, dar diferă în proprietățile fizice și chimice, numite izomerie
12 Tipuri de izomerie: izomerie a scheletului de carbon izomeri de poziție dublă (triplă) obligațiuni regioizomerii izomerie Interclass
schelet atom de carbon primar 13 izomerie carbon secundar NA NA atom Terțiar atom de carbon atom de carbon cuaternar NA carbon C
14 Formula structurală Deployed N N N N N N - C - C - C - C - C - n n n n n n redus pentan HC- CH-CH- CH CH CH Moleculară
Izomerie schelet de carbon 15 CH-CH-CH-CH-CH n pentan CH-CH-CH-CH2-metil butan CH CH C-CH 2,2dimetil propan CH
Găsiți izomeri 16 CH-CH-CH-CH-CH-CH-CH-CH-CH-CH CH CH CH-CH-CH-CH CH CH-CH-CH-CH-CH
17 Munca independentă Crearea și dau nume pentru izomerii octanică și Dean. Tema de casă 1.Vyuchit formula seriei omoloage 2.Sostavit și dau nume pentru izomerii nonanului. 3.Sostavit formula structurală: 2,2,3,5 tetramethylheptane dibutil 4,5,5,7,7pentaetildekan 2,3, 4,5,6 trimetiloktan