Neutralizarea - studopediya
Apele uzate cel mai adesea contaminate cu acizi minerali: sulfuric H2 SO4. Azotic HNO3. HCl clorhidric, precum și amestecuri ale acestora. Mult mai puțin frecvent în HNO2 de canalizare de azot. acid fosforic H3 PO4. sulfuros H2 SO3. hidrogen sulfurat H2S, HF fluorhidric, H2 SrO4 acid cromic precum și acizi organici: acid acetic CH3COOH, picric HOC6 H2 (NO2) 3. Cărbune H2 CO3. salicilic C6 H4 (OH) 2 și altele.
Apele uzate care conțin acid mineral sau alcaline, înainte de a fi evacuate în apele de suprafață sau neutralizate înainte de utilizare în procesele industriale. Practic considerata apa neutra având un pH = 6,5-8,5.
Se aplică următoarele metode de neutralizare:
1) neutralizarea reciprocă a apelor uzate acide și alcaline prin amestecare;
2) reactivi de neutralizare [soluții acide, var nestins CaO, Ca varul stins (OH) 2. sodă calcinată Na2 CO3. Caustic soda NaOH, amoniac NH4 (OH)];
3) filtrarea prin materiale de neutralizare: var, calcar, CaCO3. dolomită CaCO3 · MgCO3. magnezit MgCO3. calcinat magnezită MgO, cretă CaCO3 (96-99%);
4) neutralizarea gazelor de ardere.
În funcție de datele brute din tabelul 3.1 pot fi desemna aproximativ o metodă de neutralizare a apei acide.
Condițiile de metode de aplicare a neutraliza apele reziduale acide
Acid conținute în apele uzate
Legendă: „+“ - aplicarea metodei este recomandată; „0“ - aplicarea metodei permise; „-“ - nu este recomandată utilizarea metodei.
O metodă de neutralizare a gazelor de ardere a apei uzate alcaline. Aplicarea gazelor de ardere cu conținut de CO2. SO2. NO2 și alți compuși pot neutraliza simultan apa uzată și pentru a curăța gazele de componente nocive.
Neutralizarea apelor uzate prin amestecarea apei reziduale acide cu alcaline. Regimurile de epurare a apelor uzate conținând acid uzat și alcaline, de obicei diferite. Apa acidă este evacuată în canalizare relativ uniform pe tot parcursul zilei și au o concentrație constantă; Apa alcalină este evacuată periodic pe măsură ce soluția alcalină este descărcată. În acest sens, pentru apele alcaline de multe ori este necesar pentru a asigura reglarea rezervorului. Apa acidă și alcalină se amestecă într-un vas (fig. 3.1), cu și fără un mixer agitator. În acest ultim caz amestecul de aer cu rata de plumb din conducta de alimentare la 20 m / s. La calcularea bubblers debitului de aer per 1 m 2 de suprafață liberă poate fi luată egală cu 3 m / min pentru o agitare slabă - 0,4, pentru o perioadă medie - 0,8, pentru intensiv - 1.
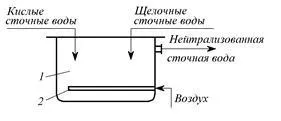
Fig. 3.1. Neutralizer de amestecare:
1 - capacitate; 2 - distribuitor de aer (barbotare)
Reactivi Neutralizarea apă uzată. Pentru a neutraliza apa acida poate fi utilizat: NaOH, KOH, Na2 CO3. NH4OH (apă de amoniac), CaCO3. MgCO3. ciment, dolomit (CaCO3 · MgCO3). Cu toate acestea, cel mai ieftin este hidroxidul de calciu (lapte de var), cu o fracție de masă de var Ca (OH) 2 5-10%. Când este vorba de eliberare nestins hidratare de căldură:
Soda și hidroxid de sodiu trebuie utilizat în cazul în care acestea sunt deșeuri. Uneori, folosit pentru a neutraliza o varietate de deșeuri. De exemplu, zgura de oțel, iar producția de furnal ferocrom este utilizat pentru a neutraliza apa care conține acid sulfuric.
Reactivii sunt selectate în funcție de compoziția și concentrația apei reziduale acide. În același timp, să ia în considerare dacă în cursul unui precipitat sau nu. Există trei tipuri de ape uzate acide: 1) apă conținând acid slab (H2 CO3 CH3 COOH) ;. 2) apă conținând acizi puternici (HCl, HNO3), pentru care orice reactivi de neutralizare menționate mai sus (o sare a acestor acizi pot fi utilizați sunt bine solubile în apă); 3) apă conținând acid sulfuric și acid sulfuros (acești acizi, săruri de calciu slab solubile în apă și precipitat).
Var pentru neutralizare este introdus în apa uzată, sub formă de hidroxid de calciu - lapte de var (dozare „umed“) sau ca o pulbere uscată (dozare „uscat“).
Când neutralizarea apelor reziduale industriale care conține acid sulfuric, reacția în funcție de reactivul utilizat curge prin ecuațiile
Sulfatul de calciu rezultat neutralizarea (gips) se cristalizează din soluții diluate sub formă de CaSO4 · 2H2 O. Solubilitatea acestei sări la o temperatură de 0-40 ° C variază de 1.76-2.11 g / l. Un dezavantaj semnificativ al neutralizarea acidului sulfuric cu gips de var este formarea unei soluții suprasaturată (factor suprasaturație poate ajunge la 4-6), selecția care din apa reziduală poate dura mai multe zile, rezultând în conducte și echipamente overgrowing. Pentru a reduce suprainfectia utilizate metode de spălare conducte crește viteza de transport și înlocuirea conductelor metalice din plastic.
Pentru a neutraliza acidul gras organic se utilizează var care conține cel puțin 25-30% oxid de calciu activ sau un amestec de var cu 25% apă de puritate tehnică.
doză de reactiv pentru tratarea apelor uzate determinată de neutralizarea completă a acizilor conținute în acesta sau alcalii și au primit 10% mai mult decât calculată (vezi Tabelul 3.2.).
Consumul de reactiv, kg / kg pentru a neutraliza 100% acizi -x și alcaline
G. reactanților kg / h, pentru a neutraliza apa reziduală este determinată prin formula
în care consumul de reactiv kz- factor de siguranță față de cel teoretic, egal cu 1,1 pentru laptele de var chit de var și var uscat 1.5; B - cantitatea părții active într-un produs de bază,%; Q - rata de ape uzate să fie de neutralizare, m 3; și - pentru a neutraliza consumul de reactiv, kg / kg (Tabelul 3.2.); A - concentrația de acid sau alcalin, kg / m3.
Prin neutralizarea apelor reziduale de acid conținut de metale grele, cantitatea de reactanți G. kg / h:
unde C1, C2, .... Cn - concentrarea metalelor din apele reziduale, în kg / m3; b1, b2, .... bn - consumul de reactiv necesar pentru traducerea metalelor dizolvate în starea precipitatului, mg / kg (Tabelul 3.3.).
Volumul Voc de nămol. %, Format în timpul neutralizării 1 m 3 apă reziduală, pot fi găsite prin ecuația
unde WVL - nămol umiditate%.
Valorile pH-ului corespunzătoare începutul și sfârșitul depunerii metalelor neferoase și hidroxizii de fier sunt prezentate în Tabelul. 3.4.
Cele multicomponente Valorile efluent pH corespunzătoare începutul și sfârșitul hidroxizilor de depunere deplasate în mod semnificativ la valori mai mari.
Este subliniat faptul că ionii de metale grele neferoase pot fi depozitate nu numai sub formă de hidroxizi, dar hidroxo-carbonat (în cazul utilizării pentru reactivii de precipitare conținând ioni de carbonat în structura sa). De exemplu:
2Ni 2+ + + 2OH - → (NiOH) 2 ↓ CO3 (3.6)
PH de precipitare a hidroxizi metalici
Zinc, aluminiu și alte metale având proprietăți amfoteri pot fi prezenți ca anioni în apa uzată alcalină. Pentru a le elimina folosind soluții acide. În această formă de hidroxid de metal precipită în conformitate cu următoarele ecuații:
Trebuie subliniat faptul că mai eficient co-precipitarea ionilor de două sau mai multe metale la același pH decât în precipitarea fiecare metal individual.
Acest lucru se datorează formării cristalelor mixte și a proceselor de adsorbție pe suprafețele lor.
In tratamentul cu reactivi alcalini apa reziduală conținând ioni de metale grele neferoase, se realizează prin reducerea concentrațiilor lor la valori care permit descărcarea apei purificate în canalizare municipale sau cursuri de apă sanitară și uz casnic.
În cazul în care un grad mai profund de curățare, metale grele, recomandat să aloce forma de sulfura. De obicei, izolat ca sulfurile de Cu, Co, Ni, Fe, Sn, Mo, As, Sb, Hg, Ag, Zn, Cd, Pb. Pentru cation bivalent reacția de formare sulfură de metal poate fi scrisă sub forma:
Me 2+ + S 2- → Mes ↓ (3.12)
Ca precipitant utilizat este de obicei Na2S (mai puțin - (NH4) 2 S).
General de ape uzate schemă tehnologică a ionilor de metale grele prezentate în Fig. 3.2.
Avantajele metodei de reactiv ar trebui să includă un grad ridicat de purificare din metale grele (sus TPM), precum și simplitatea echipamentului. Principalele dezavantaje ale metodei - este o cantitate semnificativă de trudnopererabatyvaemogo nămol, precum și un consum substanțial de reactivi și nevoia asociată organizării plantelor chimice. Mai mult, această metodă apă purificată conține o cantitate substanțială de săruri, și pot fi utilizate în sistemele de apă care circulă numai după purificare.
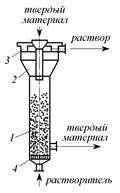
Var hidratat este produs în unitatea de coloană (fig. 3.3). Coloana cilindric 1 prin duza inferioară alimentată continuu de lichid care este filtrat printr-un strat de material se deplasează în jos. O soluție din concentrația necesară a părții lărgite 2 a coloanei, care joacă un rol de separator iese prin unitatea de montare laterală pentru prelucrare ulterioară.
Fig. 3.2. reactiv apă reziduală din schema tehnologică ionii de metale grele
Materialul sub formă de particule solide de pornire este alimentat continuu prin tubul de alimentare, reziduul nedizolvat a fost retras din partea de jos. Dispozitivul poate funcționa într-un pat în mișcare dens sau într-un mod în pat fluidizat. Caracteristici distinctive sunt eficiență ridicată volumetric și simplitatea dispozitivului.
La prepararea soluției de lucru a laptelui de var amestecare soluție acceptabilă a aerului la intensitatea aerării de 0,8 m 3 / (m 2 · min), agitarea este de asemenea posibil pompe hidraulice prin capacitatea rezervorului de 1-4 m 3.
Pentru distribuirea reactanti de pulberi uscate dozatoare folosite în alte industrii utilizate (materiale de construcții, produse chimice, etc ..).
Pentru decantare precipitarea neutralizare rezultată se aplică jompuri destinate să rămână în apele reziduale sunt de cel puțin 2 ore pentru a ajusta pH-ul la 7,5-8,5.
Deshidratarea nămolului pe un filtru cu vid este furnizat într-o cantitate de substanță uscată în ea de cel puțin 25 kg / m3.
La calcularea sarcinii pe filtru cu vid trebuie sa fie 15-25 kg / (m2 · h), frecvența de rotire a tamburului de 0,4 min -1. sprijinit 53-80 kPa în vid; ca pânza de filtru utilizat de nylon și curelele.