cataliza heterogena 2
Izolatori: catalizatori acizi și bazici.
Catalizatorii aparținând acestui grup, nu conduce electricitatea (cel puțin la temperaturi relativ moderate cataliză), adică nu sunt electronii se deplasează liber și, prin urmare, în mod substanțial, nu catalizează reacții redox.
De exemplu, oxizi solizi ai elementelor treia perioadă (Na2 O, MgO, Al2 O3. SiO2. P2 O5) sunt izolatoare. După cum se arată în acest rând, de la stânga la dreapta oxizi proprietăți variază de la bază la amfoter acide prin. În mod similar se comportă oxizi de alte perioade.
Chemisorpția care apar în taxele pe suprafața catalizatorilor, izolatori nu sunt transmise pe catalizator și localizate în centrele activă. Prin urmare, proprietățile catalitice ale izolatori nu pot fi explicate în mod satisfăcător teoria electronilor, iar cel mai potrivit concept pentru explicarea proprietăților catalitice ale izolatorilor este conceptul de acizi și baze.
Bine cunoscut și cel mai utilizat în sinteza industrială a catalizatorilor acizi baze organice includ: Al2 O3. aluminosilicați, zeoliți, MgO, SiO2 / MgO, dioxid de siliciu, aluminofosfați și argile speciale, activate prin tratament chimic.
Toți acești catalizatori cuprind pe siturile acide de suprafață.
Raportul principalelor catalizatori heterogeni industriale este mult mai mică decât cea a acidului. Tabelul 5.21 prezintă cunoscuți catalizatorii acido-bazic.
Clasificarea catalizatorul acid-bazic.
catalizatori acizi eterogeni
catalizatori heterogeni de bază
oxizi micsti: 2O 3 / SiO2. SiO2 / MgO, ZrO2 / SiO2. heteropoliacid (fosfowolframic, fosfomolibdenic).
Acid mineral (H3 PO4. H2 SO4) pe suporturi poroase solide.
Materiale polimerice schimbătoare de cationi.
Săruri oxigena acizi minerali (fosfați, sulfați, wolframite) și metale de tranziție.
Halogenuri cu acid Lewis (AlCl3) de pe suportul poros solid.
Zeoliții (în forma H).
Superacid: ZrO2. TiO2 tratate cu acid sulfuric.
Oxizii, hidroxizi, amide, metale alcaline și alcalino-pământoase (per se și pe medii solide).
Polimerica material schimbător de anioni.
Sărurile alcaline și alcalino-pământoase ale acizilor slabi (carbonați, silicați).
Superbases: MgO dona sodiu.
Catalizatorii de oxid având suprafață acidă catalizează multe reacții industriale importante (deshidratarea alcoolilor, hidratarea olefinelor, fisurare, polimerizarea olefinelor, condensarea compușilor carbonil, esterificare și așa mai departe.).
site-uri de pe suprafața acide de oxid solid poate avea atât aciditate protic (Bronsted) sau acid aprotic (Lewis) (A se vedea. P. 2.1.1).
Luați în considerare natura protic și aprotic siturilor acide de pe exemplul de alumină. Al2 O3 apă legată conține întotdeauna o cantitate care depinde foarte mult de temperatură. Proaspăt preparată (-precipitated) Al2 O3 hidroxilat complet la suprafață până la o temperatură de 100 C. In aceasta stare, grupările -OH de suprafață se comportă ca acid slab Bronsted:
crește în mod semnificativ Broensted centre de aciditate cutie inlocuind o parte din grupările hidroxil clorura sau anion fluorură (tratarea cu o halogenură de hidrogen corespunzătoare):
Creșterea acidității grupei OH, datorită efectului inductiv puternic de halogen-vnionov, aproape gruparea -OH.
Când este încălzit, temperatura de alumină hidroxilat peste 150 ° C, deshidratarea suprafeței și aproape de suprafață -OH grupuri. În această formă dehidroxilați atomii de aluminiu pe suprafața cu acidul Lewis mediu:
Concomitent cu formarea centrelor de Lewis acidității Bronsted îmbunătățită adiacente centrelor datorită unei posibile interacțiuni donor-acceptor de tipul următor:
La o temperatură de 400 ° C și are loc deasupra dehidroxilare atomii de aluminiu de suprafață, pentru a forma un acid Lewis puternic și centre de bază:
La o temperatură de 900 ° C suprafață Al2 O3 complet și dehidroxilare conține numai centre acide și bazice Lewis.
Reglementarea raportului și a forței protic și centre acide aprotici și centrele de bază pe suprafața Al2 O3 este foarte importantă pentru a asigura efectul catalitic optim într-o anumită reacție. Sa constatat că puternice centre de acid Bronsted joacă un rol crucial pentru reacțiile de polimerizare a olefinelor, disproporționarea toluen la benzen și xileni. site-uri acid Lewis sunt cruciale în reacția de degradare a alcanilor.
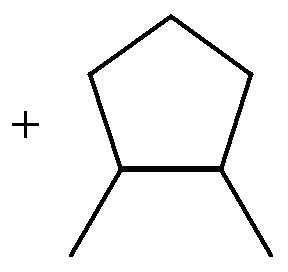
Ciclizarea olefinelor în reformarea are loc procesul de cataliză convenit adiacent - proton bazic și acid - centre de pe suprafața de alumină:
acțiunea catalitică eterogenă a acizilor și bazelor este aceeași cu cea a omogenului. Activitatea catalitică corelată cu aciditatea siturilor active în conformitate cu ecuația Bronsted:
Valorile centrelor funcționale aciditate pe suprafața unui catalizator eterogen poate fi obținută experimental:
sau cu ajutorul unor indicatori Hammett;
sau spectrele IR ale bazelor adsorbiți cum ar fi amoniacul, piridină, chinolină.
A doua metodă se bazează pe faptul că complexele de baze selectate și acizi Bronsted Lewis au structuri diferite și, prin urmare, au o bandă de absorbție caracteristică la diferite regiuni spectrale. Numărul total de locuri de acid este determinată de cantitatea de amoniac adsorbit chimic. Apoi, intensitățile de semnal în spectrul IR este posibil să se determine raportul dintre concentrațiile de centri acizi protici și aprotici pe suprafață și pe semnalul de deplasare - forța centrele respective.
De exemplu, o suprafață de compus și frecvențele caracteristice corespunzătoare din spectrul IR atunci când este utilizat ca „sondă“ piridină următoare:

dioxid de siliciu (silice) este amorfă policondensat acid silicic cu grupările silanol (Si-OH) și formarea de grupe siloxan (Si-O-Si):
Comunicarea cu grupările hidroxil de suprafață de atomi de siliciu în SiO2 este mult mai puternică decât legătura cu grupele hidroxil ale atomilor de aluminiu din Al2 O3. De aceea, deshidratarea silicei la temperaturi de până la 120 ° C, însoțită de o pierdere doar apa adsorbit fizic. Dehidroxilare suprafețelor de siliciu începe numai la temperaturi de peste 200 ° C La o temperatură de 500 ° C, concentrația grupărilor silanol de suprafață este de aproximativ 20-30% din original, iar la 1000 ° C - 10-15%.
Astfel, spre deosebire de alumină pe suprafața centrelor SiO2 Lewis sunt formate nu atât de ușor, și la temperaturi de până la 300 ° C este, practic, detectată. Prin urmare, pe suprafața de oxid de siliciu este dominată de centre Bronsted, dar aciditatea lor este scăzută și comparabilă cu aciditatea acidului acetic. De aceea, silicea în sine drept catalizator nu este de interes, dar este purtător valoros, deoarece are o suprafață specifică mare (800 m2 / g).
Aluminosilicați - una dintre cele mai importante tipuri de catalizatori acizi eterogeni utilizate în procesele de cracare.
Chimic, ele reprezintă o silice, în care o porțiune din atomii de siliciu înlocuiți cu atomi de aluminiu. ion de aluminiu trivalent la suprafață este înconjurată de trei ioni de siliciu quadruply având o electronegativitate mai mare. Aceasta are ca rezultat o scădere puternică a densității de electroni pe atomul de aluminiu și, prin urmare, pentru a crește electrofilie sale (de aciditate Lewis). Ca urmare, moleculele de apă sunt pe suprafața chemisorpția disociative aluminosilicat:
rezultând în formarea unui situs de acid proton puternic. Atunci când este încălzit la temperaturi ridicate, deshidratarea suprafeței și formarea unei puternice situri acid Lewis (revers reacție (5,64)).
aluminosilicați acidității puternice furnizate la o concentrație de Al2 O3 10-12%. Sa stabilit experimental că aciditatea maximă este observată la o concentrație de 20-30% din Al2 O3.
O creștere a acidității aluminosilicat poate fi realizată prin tratarea cu o cantitate mică de HCl:
pe suprafața aluminosilicați și raportul lor de distribuție de putere a concentrațiilor de situri acide și Bronsted Lewis raportul ajustat SiO2 / Al2 O3. Temperatura de proces obrabotkoyHCliNa2 O. Astfel reglează fin administrează activitatea și selectivitatea catalizate.
Zeoliții, spre deosebire de Al2 O3, silicați SiO2 și aluminiu care sunt substanțe amorfe - sunt substanțe cu conținut de apă, cu structură cristalină foarte ordonată. Unitatea de bază a zeoliților este un tetraedru de patru anioni de oxigen din jurul ionSi 4+ sau Al 3+ (Fig. 5.49). taxa Silicon fiecărui ion este echilibrat taxele din jur ioni de oxigen și, prin urmare, conțin siliciu tetraedre - electric neutru. Un aluminiu tetraedru care conține exces taxa de -1, drept cation de aluminiu are o sarcină de +3. Prin urmare, compoziția include zeoliti cationi pentru a compensa sarcina negativa. Tetraedrele sunt combinate în blocuri privind comunicațiile -Si-O-Si-, care este construit din structura zeolitului. In general, compoziția chimică a celulei unitate zeolitul prezintă formula:
unde: M - cationi, de obicei alcaline și alcalino-pământoase metalelor; j - numărul de cationi de aluminiu într-o celulă; n - taxa de M cation (deci j / n - numărul de cationi M, necesară pentru a compensa sarcina negativă a tetraedrului de aluminiu); Y- cantitatea de ioni de siliciu; Z- cantitatea de apă de hidratare.
Simplist structura de suprafață de Na care conține zeolit este prezentat în figura 5.50-a. Dacă sodiu este înlocuit cu un proton, obținem zeolit în forma H + (Fig. 5,50-b.).

Fig. 5,49. tetraedre și siliciu conține aluminiu în structura zeolit.
Fig. 5.50. suprafață zeolit: și - în forma Na; b - în forma H.
Prin reglarea sintezei raportului zeoliți Si / Al, natura cation M, gradul de substituție al M de H + și adâncimea elimina apa de hidratare aciditatea zeolitului poate fi modificată în limite foarte largi. De aceea, zeoliții sunt de tip valoroase și utilizate pe scară largă de catalizatori acizi în chimia organică industrială.
Datorita proprietatilor sale unice, utilizarea zeoliti în cataliza nu este limitată. Mai multe detalii zeoliti vor fi discutate separat în clauza. ***.
Mecanismele reacțiilor care apar pe suprafața catalizatorilor acizi.
deshidratare intramoleculară și intermoleculară.
Catalizatorii acizi accelera atât deshidratare intra- și intermoleculare hidrocarburilor hidroxilați. Activitatea și selectivitatea catalizatorilor (în plus față de condițiile procesului) depinde de aciditatea suprafeței.
Comportamentul de oxid de aluminiu în deshidratarea etanolului.
Relativă aciditate * (175 ° C)
* - mmol NH3. adsorbit 1 gram de Al2 O3.
Să analizăm datele din tabelul 5.22. Creșterea conținutului de SiO2 duce la creșterea aciditate Bronsted. Creșterea conținutului rezultatelor Na2 O în neutralizarea siturilor puternic acide Broensted și de a stabiliza centrele de bază. Evident, aciditatea totală a probelor crește odată cu creșterea conținutului de SiO2 și o scădere a soderzhaniyaNa2 O.
Sa constatat că deshidratarea etanolului se produce la protoni acizi comune de acțiune și siturile catalitice de bază:
Prin urmare, cea mai mare activitate și selectivitatea etilenei se observă pe proba cu aciditatea medie (raportul optim de locuri de bază și acide). Proba cu cea mai mică aciditate are cea mai scăzută activitate (conversie) și selectivitatea inferioară a etilenei. În plus, sa constatat că deshidratarea are loc la site-uri de acid Bronsted de putere moderată, și centre Lewis, practic, nu a cataliza această reacție. Această concluzie se bazează pe faptul că adăugarea unor cantități mici de baze Lewis (amoniac, piridină, etc.), blocând primul puternic acid și centrele aprotici nu inhibă reacția.
Un punct important în acest exemplu - formarea de cocs. După cum se poate observa crește cantitatea de cocs proporțional cu aciditate Bronsted. Acest lucru se datorează faptului că la aceste centre carbocationilor intermediare formate initierea dimerizarea si oligomerizarea etilenei. Depunerea de produse nevolatile ale rezultatelor oligomerizare într-o suprafață de blocare, o reducere a activității catalitice și cocsarea.
Reacțiile în reformarea și cracare catalitică (cracare, izomerizarea, polimerizare, ciclizare, aromatizarea, cocs)
Etapa cheie asigurarea activității catalitice a catalizatorilor acizi în reacțiile de cracare, izomerizare, polimerizare, ciclizare, aromatizarea, formarea cocsului este formarea carbocationilor prin reacția unei hidrocarburi cu centrele de suprafață activi.
Formarea carbocationului poate avea loc prin trei mecanisme:
Separarea anion hidrură de ceară puternice centre de acid Lewis:
Site-uri protonare parafină Bronsted acid pentru a forma hidrogen și un carbocation. O astfel de reacție este posibilă numai cu participarea centrelor Bronsted foarte puternice, de exemplu, lângă Lewis Center ((5.59) (5.64)):
Olefinele sunt necesare pentru reacția (5.69) pot fi prezente în materiile prime, ca impuritate, pentru a forma ca rezultat al cracarea termică sau cracarea carbocationilor rezultate formate la situsuri catalitice asupra reacțiilor (5,67), (5,68). Cracare neramificate veniturile carbocationi secundare conform schemei:
Rezultat carbocationului primar poate regrupa într-un terțiar secundar sau mai stabil.
Un posibil mecanism ciclizare și aromatizarea hidrocarburilor la catalizatori acizi pot fi reprezentați prin următoarea schemă. Olefinele hidrură capabilă să dea un anion de alil centri acizi ai catalizatorului, pentru a forma un krbokationa alilic stabilizat cu rezonanță:
Carbocationului rezultată poate dona un centru de protoni suprafață catalitic principal pentru a forma o dienă de:
Mai mult, conform aceluiași mecanism poate fi format trienă care ciclizează ușor sub siturile de acid catalizei protoni:
Diena ciclică rezultată atunci când transformat într-un carbocation prin reacția cu un alt carbocationului pe suprafața catalizatorului:
Mai mult, catalizatorul principal dând centru proton krbokation transformat într-o hidrocarbură aromatică:
Ciclizarea poate să apară ca rezultat al carbocation atac electrofil intramoleculară având o dublă legătură:
După cum se vede din schemele de mai sus aromatizarea hidrocarburilor are loc pe catalizatori acizi cu principalele centre. Dar, ca principalele centre de activitate ale catalizatorilor acizi este scăzută, reacțiile de aromă se desfășoară încet. În cracarea catalitică a fracțiunii de motorină a hidrocarburilor aromatice în produsele este de aproximativ 2%.
reacție catalitică acidă izomerizării, polimerizare, alchilare, transalchilare (disproporționare) pe catalizatori heterogeni proceda prin aceleași mecanisme ca și în cataliza omogenă a unui acid.
Formarea cocsului pe suprafața catalizatorului acid se datorează în principal reacției de condensare catalizate cu acid a compușilor aromatici. O schemă simplificată poate fi reprezentată după cum urmează:
Aromatice polinucleare carbocationului foarte stabil, prin urmare, ea poate nu numai să doneze un proton pentru a forma compuși polinucleari:
dar, de asemenea, să continue reacții de condensare în continuare în lanț pentru a forma cocs. Această schemă simplificată a reacțiilor de formare a cocsului poate fi urmată de alchilare, polimerizare, ciclizare.
Aciditatea catalizatorilor și reactivitatea.
In reacțiile care apar numai la locurile de acid (de exemplu o polimerizare olefină) activitate se corelează cu aciditate de suprafață (Bronsted conform ecuației).
Experiența arată că cea mai mare aciditate se realizează pe amestecuri de oxizi, în care cationii au un număr diferit de coordonare (sau starea de oxidare). Tabelul 5.23 prezintă oxizi mixte cu o gamă largă de aciditate de suprafață. Activitatea catalitică a catalizatorilor acizi eterogeni corespunde omogene acizilor minerali activitate catalitică cu aceeași valoare pH. Dar acest catalizatori heterogeni au avantajul de stabilitate termică și ușurința separării de masa de reacție.
Rezistența centrilor acizi de oxizi binare.