Proprietățile soluțiilor de polielectroliți
Pentru polyelectrolytes sunt cele mai importante biopolimerilor - proteine și acizi nucleici.
Polyelectrolytes acești compuși macromoleculari care conțin grupe ionice macromoleculă polare. Polyelectrolytes pot disocia în ioni în soluție.
stat izoelectrică
H
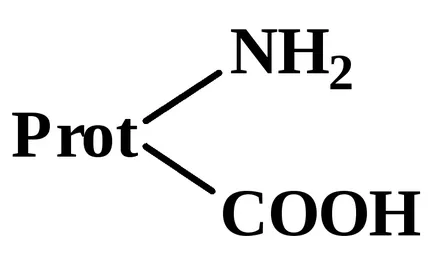
semn al taxei macromoleculei depinde de:
Cantitățile și natura grupărilor funcționale libere, cum ar fi raportul dintre carboxil și grupările amino din molecula de proteină.
În cazul în care macromolecula este dominat de grupări de acid carboxilic, apoi la pH = 7 sarcina negativă a moleculei (proprietăți manifeste de acid slab), în cazul în care gruparea amino predominantă a proteinei sarcinii pozitive (proprietăți caracteristice de bază)
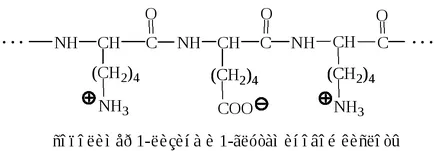
Condițiile de viață ale organismului proteine de obicei, prezintă proprietăți anionice, prin care eritrocite și suprafața celulei are o sarcină negativă.
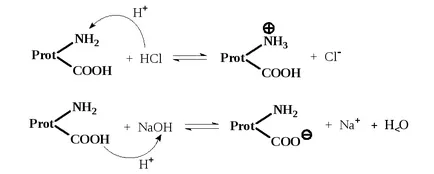
Condiția în care numărul de sarcini opuse în aceeași moleculă de proteină, adică taxa net polyampholyte este zero, nazyvaetsyaizoelektricheskim. PH-ul corespunzător soluției de stat izoelectrice se numește punctul izoelectric (pI sau IT). Intr-un mediu cu bólshey acid decât punctul izoelectric (pH
Astfel, atunci când pH-ul soluției <рI, белок имеет положительный зарад; при рН раствора> pI, proteina are o sarcină negativă. De exemplu, pentru a determina încărcătura următoarelor proteine într-o soluție cu pH = 8,5: gastric din sange pepsină nucleele celulare histone și lizozimul.
r
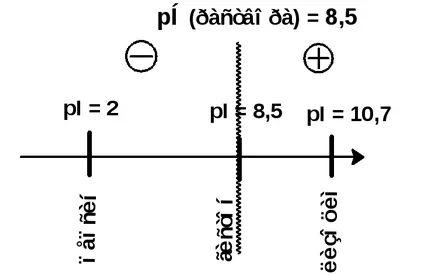
pI (histonă) = 8.5. deoarece pH egal cu pI, proteina este neutră,
pI (lizozimul) = 10,7, deoarece pI mai mare pH, proteina are o sarcină pozitivă.
Proprietățile soluțiilor de proteine în stare izoelectrică.
starea izoelectrică afectează structura proteinelor și a soluțiilor lor. Pentru punctul izoelectric al proteinei se caracterizează prin coagulare a macromoleculelor în bile; în starea încărcat de lanțuri de proteine au o formă alungită.
Reprezentarea schematică a structurii proteinelor:
și
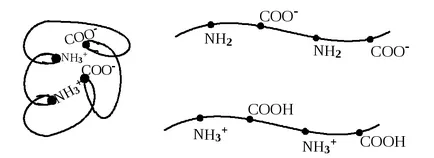
b) Structura rotundă fibrilare cu o sarcină negativă (pH> pI);
a) structura fibrilară cursei, cu o sarcină pozitivă (pH În plus, în starea izoelectric scade coajă de proteine solvatare nu este inutil de puternic solvatare electrostatic. Prin urmare, în apropierea punctului izoelectric poate fi modificări de bază ale proprietăților proteinelor, și soluțiile lor. Deoarece punctul izoelectric de conductivitate scăzută electrice, stabilitate și umflarea proteinelor, precum vâscozitatea și osmolalitatea soluțiilor de proteine și procesele de coagulare și gelificare maximale.