ocuparea forței de muncă practic № 5
Alocări. 1. Se obține marmura dioxid de carbon, prin reacția cu acid clorhidric.
2. Exploreaza unele proprietăți fizice ale dioxidului de carbon (IV) (culoare, miros, solubilitate în apă, greutate specifică).
3. a) Interacțiunea de dioxid de carbon cu apă, b) efectuează următoarea conversie;
4. Recunoasteti calcar Printre exemplarele minerale remarcabile.
5. Ia-carbonat de bariu prin metateză.
Echipamente. Dispozitiv pentru gaze, bucăți de marmură condimentată și acid clorhidric, trepied laborator stativ cu eprubete, pipete, paharelor cu 150 ml (2 buc.), Cartonul cerc la probirkoderzhateli din sticlă (2 buc.), Heater.
Substanțe. O soluție 10% de carbonat de sodiu și clorură de bariu, acid clorhidric 10%, apă de var, soluție de turnesol, apă distilată, minerale, gips, caolin, calcar, cuarț.
1. Prepararea oxidului de carbon (IV). Încărcați dispozitivul pentru producerea dioxidului de carbon (Fig. 22.4). Ia-dioxid de carbon, se pune într-un pahar și se acoperă cercul de carton. (De ce?)
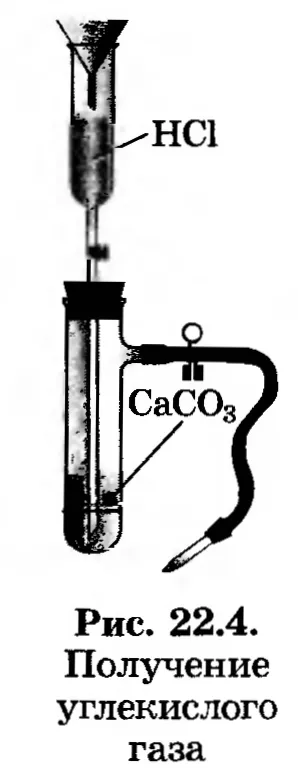
2. Studiul proprietăților oxidului de carbon (IV). Fă un chibrit aprins de sticlă. Ce să Uita-te? „Se toarnă“ conținutul într-un alt pahar. Asigurați-vă cu ajutorul unei partide de ardere, care dioxidul de carbon nu „overflow“ de la un pahar la altul.
Ce proprietăți de dioxid de carbon este baza acestei experiențe? Descrie proprietățile fizice ale gazului de testare.
Se toarnă tub (1/4 din volumul său) apă distilată tentă violet tracțiune sale
turnesol hoț și trecut prin dioxid de carbon de apă pentru a schimba culoarea indicatorului. De ce schimba culoarea de turnesol? Asigurați ecuația reacției corespunzătoare. Se încălzește conținutul tubului înainte de începerea fierbere. De ce schimba culoarea de turnesol din nou? Explicați-l cu ajutorul ecuației de reacție.
3. Tub tide (1/4 din volumul său) și apă de var sări peste dioxid de carbon prin acesta. La ce te uiți? În cazul în care este folosit în practica acestei reacții? Continuă să treacă de dioxid de carbon printr-un amestec tulbure până clarifica complet soluția. Ce sa întâmplat? Asigurați-ecuația reacțiilor observate.
Conținutul tubului de testare cu carbonatul de calciu obținut este împărțit în două părți egale. Intr-un tub, se adaugă apă de var și alte tipuri de căldură înainte de soluția de fierbere. La ce te uiți? Explicați ce se întâmplă fenomen cu ajutorul ecuației de reacție. Egal concluzii: a) modul în care carbonații pot fi transformate în hidrocarburi și b) cum să transforme bicarbonații în carbonați.
4. Pentru că a emis minerale prin reacții chimice determina calcar. Asigurați ecuațiile ionice efectuate de reacție.
5. Ia reacția de schimb de carbonat de bariu. Empiric dovedesc că precipitatul este într-adevăr carbonat. Asigurați-vă ecuații lungi și scurte ionice ale reacțiilor efectuate.
Carton sticlă acoperire cerc nu volatilizează dioxid de carbon.
Atunci când face un pahar cu meci de dioxid de carbon se stinge, deoarece Dioxidul de carbon nu acceptă arderea. Dioxidul de carbon poate fi turnat dintr-o cana la alta, deoarece este mai greu decât aerul și se sedimentează pe partea de jos.
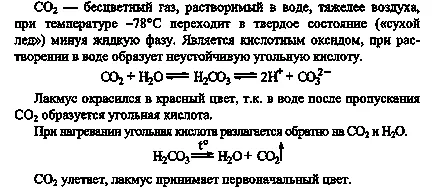
turbiditate Există de soluție, în practică, este utilizat în pereții Ceruza. Reacția are loc:
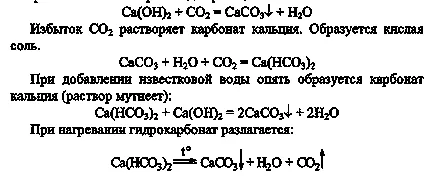
a) carbonați pot fi transformați în hidrocarburi prin trecerea acestora prin dioxidul de carbon;
b) hidrocarburile pot fi convertite în carbonați prin încălzire sau prin adăugare de apă de var.
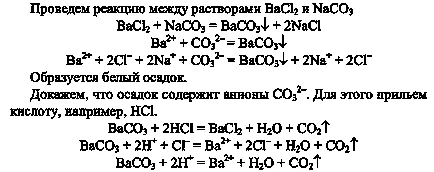
Cu condiția de gaz care nu suportă arderea.