Metode de producere - studopediya
1. Hidroliza galogenproizvodnyh:
2. Reducerea aldehidelor aromatice:
3. Reacția Konnitstsaro. Acțiunea pe un amestec de două aldehide soluții de alcalii concentrate pentru a se obține alcoolul și acid:
4. Sinteza hidrocarburilor aromatice și oxizi cu clorură de aluminiu drept catalizator:
Proprietăți chimice și aplicare. Alcooli cu o grupă hidroxil în # 945; - poziția reacționează ușor gidrogalogenirovaniya (SN):
Alcooli cu o grupă hidroxil în # 946; - poziția deshidratează ușor (E):
Alcool benzilic ca esteri ai acizilor acetic și benzoic utilizat în parfumerie. Esterii alcoolului benzilic și cinamic și acizii benzoic fac parte din uleiuri naturale, balsamuri, provoacă mirosul de iasomie, zambila, tuberoze.
# 946; -feniletilovy alcool gasit in ulei de trandafir este utilizat în parfumerie, ca un miros de stabilizator.
Fenoli - molecule hidroxi în care grupele hidroxil sunt legați direct la inelul benzenic.
Fenolii în funcție de numărul de grupe hidroxil sunt împărțite în una, două, trihidric și polihidroxilici:
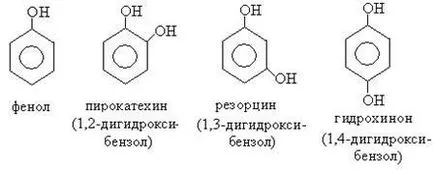
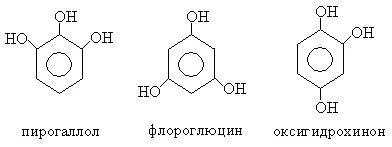
Fenolii sunt fie nume banale, sau ele sunt cunoscute sub numele de benzen substituit.
Structura fenolica sub formă de glucozide incluse în țesutul plantei.
Metodele de preparare. Există mai multe metode de introducere a unei grupări hidroxil în ciclul aromatic. Unele dintre ele au aplicații industriale:
1. Fuziunea a sărurilor de sodiu ale acizilor sulfonici cu baze:
2. Din gudron de producție de cocs fluid.
3. Hidroliza derivaților cu halogen. Tehnica de fenol obținut cu un randament bun din hlobenzola. Procesul are loc în condiții stricte, ca clorul asociat cu miezul este inactiv:
4. oxidativă decarboxilarea acizilor carboxilici:
5. Procedeu comun pentru prepararea fenolului și acetonă (Metoda Sergeev Kruzhalova-Nemtsova):
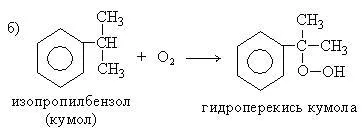
6. Prepararea aminelor din fenol prin diazotizare (reacția Sandmeyer):
7. derivați de fenol fac parte din uleiurile esențiale:
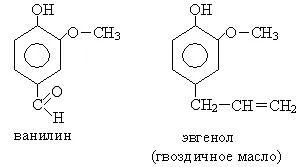
Proprietăți chimice. Principalele centre de reacție în fenol este o grupă hidroxil și un inel benzenic aromatic. Prin urmare, reacțiile tipice sunt:
- reacția unei grupări hidroxil;
- substituția electrofilă pe inelul benzenic.
I. Reacția unei grupări hidroxil.
1. Proprietăți acide bazice ale fenol. Proprietățile acide ale fenolului (abilitatea de a dona un proton) exprimat în mod semnificativ mai puternică decât alcoolul. Acest efect se datorează electronic oxigen perechi de cuplare în fenol cu un inel benzenic aromatic. Rezultat sarcina negativa asupra nivelului de oxigen este mult mai mic și un proton este ușor de rupt. În alcooli acest lucru nu se observă, deci fenolul numit și acid carbolic.
Înalta Aciditatea fenolului îi permite să interacționeze nu numai cu metalele active dar și cu hidroxizi de metale alcaline.
2. Interacțiunea cu alchine galogidnymi:
3. Interacțiunea cu acid cloracetic:
4. Interacțiunea cu cloruri acide:
5. Interacțiunea cu anhidridele acizilor carboxilici:
II. reacții de substituție electrofilă în ciclul benzenic.
Influența reciprocă a atomilor din molecula de fenol se manifestă nu numai în comportamentul grupărilor hidroxil, dar, de asemenea, o mai mare reactivitate a inelului benzenic. Gruparea hidroxi mărește densitatea de electroni a nucleului benzenic, în special în pozițiile orto și para (M + -effect grupe OH);
Prin urmare, în mod considerabil mai activ decât fenol benzen reacționează substituție electrofilă (SE), pe inelul aromatic.
1. Halogenarea. Fenolul ușor la temperatura camerei, a reacționat cu apă de brom pentru a forma un precipitat alb de 2,4,6-tribromfenol (răspuns calitativ la fenolul):
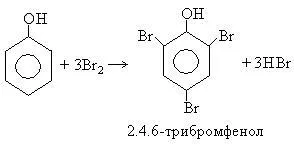
2. reacția de nitrare. Sub acțiunea 20% fenol acid azotic este ușor transformat într-un amestec de orto- și para-nitrofenoli. nitrofenoli izomere separate cu ușurință datorită faptului că numai izomerul orto este volatil cu abur. Volatilitatea ridicată a orto-nitrofenoli explicată prin formarea de legături de hidrogen intramoleculare.
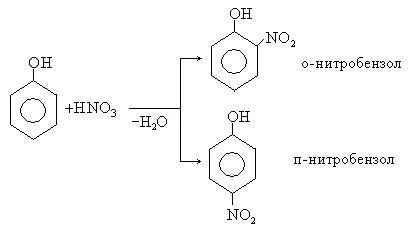
Utilizarea de HNO3 concentrat, format 2,4,6-trinitrofenol (acid picric)
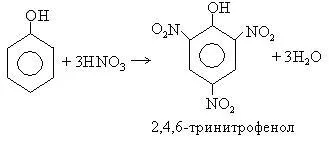
3. sulfonare fenolilor obținut o - și p -fenolsulfokisloty. La temperatura camerei, acid sulfuric concentrat în principal dă aproximativ izomerului, în timp ce la 100 C 0 p izomerul- predomină. Izomerii sunt separați datorită diferite solubilitatea sării de bariu:
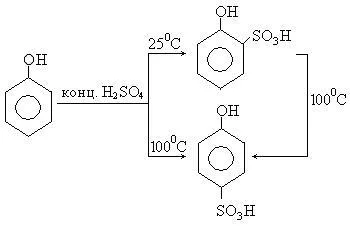
Utilizarea fenolului și a derivaților săi. Fenol - substanță cristalină are antibacteriene, proprietăți dezinfectante și intitulat carbolic acid este utilizat în medicină. Fenol face arsuri profunde și grave pe corpul său. Utilizate pentru producerea de rășini fenol-formaldehidă:
rășini fenolformaldehidice sunt numite bachelită. La efectuarea polimerizării rășini novolochnye sunt preparate în condiții acide, care sunt caracterizate printr-o structură liniară, în care condensarea are loc în poziția orto a fenolului. În mediu alcalin obținut rezol caracterizat prin reticulare moleculele pozițiile orto și para. Această reacție de condensare este o reacție de substituție electrofilă, carbonul electrofilă al grupării carbonil protrudes aldehidă.
Fenolii ca glicozide larg distribuite în natură, de exemplu, Arbutin, care este conținut în frunzele și semințele de pere. hidroliza enzimatica a Arbutin, hidrochinonă este format, care prin oxidare conferă specific negru. Aceasta explică innegrirea frunzelor în pere de toamnă.
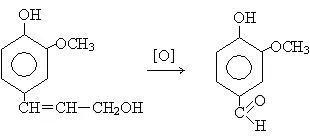
Compușii fenolici sunt parte a ligninei și conținea aproape toate plantele. Coaja de stejar conține până la 20% compuși fenolici. În onoarea acestei plante, care este una dintre primele și destul de bogată sursă de compuși fenolici, au fost numite taninuri. Buchet coniac în vârstă este cauzată de oxidarea derivatului fenol - alcool coniferil la vanilină, care informează aroma caracteristică.
fragment fenolic intră în componența antociani - structurile care conduc la o paletă de culori bogată de culori diferite. În funcție de natura radicalii R1 și R2 pot fi diferite culori.
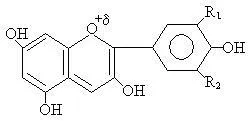
- Cyanidin (culoare cornflower)
Structuri fenolice fac parte din taninuri (acid galic este conținută în coaja de stejar si salcie). Astringență datorită prezenței de catechine de ceai.
fenoli dihidrici sunt utilizate ca antioxidanți. Mecanismul de acțiune este următoarea:
antioxidanți fenolici sunt utilizate pe scară largă în industria alimentară pentru a preveni alterarea de grăsimi, uleiuri și creme. Cele mai frecvente dintre acestea sunt:
2-terț-butil 3-terț-butil 2, 6- di-terț-butil
4- metoxifenol 4-metoxifenol 4 - metoxifenol