mecanisme comune de insuficiență cardiacă
forma miocardică de insuficienta cardiaca caracterizata prin reducerea tensiunii dezvoltate de inima. Aceasta este forța toamna și viteza de manifestat contracție și relaxare.
forma de suprasarcină de insuficiență cardiacă este generată în timp ce perioada de mai mult sau mai puțin lung a hiperfuncției sale. Acesta din urmă în cele din urmă duce la o scădere în puterea și viteza de contracție și relaxare a inimii.
În ambele cazuri (și, în caz de suprasarcină, și deteriorarea cardiace) reducerea funcției sale contractile însoțită de includerea intracardiacă extra- și a compensa acest lucru mecanisme de schimbare. Toate acestea, în ciuda identității bine-cunoscut, în ceea ce privește întregul organism sunt interconectate în așa fel încât activarea unuia dintre ele afectează în mod semnificativ punerea în aplicare a celuilalt.
Mehanizmyekstrennoykompensatsiisokratitelnoyfunktsii
Mecanisme suplimentare de plată funcției contractile redusă a inimii sunt prezentate în Fig. 22-25.

Fig. 22-25. mecanisme de compensare suplimentare a redus funcției contractile a inimii.
• contractilității miocardice crescută sub tensiune inflowing din sânge (mecanismul Frank -Starlinga). Acesta prevede o creștere a tensiunii dezvoltat de miocard și viteza de contracție și relaxare.
† Creșterea tensiunii inimii în curs de dezvoltare, efectuate ca răspuns la tensiunea tot mai mare a miocardului. În acest sens, un mecanism numit Frank -Starlinga geterometricheskim, adică asociată cu o creștere a lungimii fibrelor musculare.
† Creșterea cardiomiocitelor contracție și viteza de relaxare se dezvoltă datorită eliberării rapide a Ca2 + din depozitele de calciu (sarcotubules) și pompare ulterioară rapidă Ca 2+ (Ca 2+ -ATPazei) în reticulul sarcoplasmic rezervor.
• Creșterea rezistenței contracțiilor miocardice, ca răspuns la sarcină crescută. Aceasta are loc la o lungime constantă a miocitelor. Un astfel de mecanism este numit gomeometricheskim, deoarece acesta este pus în aplicare, fără a schimba în mod semnificativ lungimea fibrelor musculare.
• O creștere a contractilității cardiace prin creșterea frecvenței cardiace.
• Creșterea contractilității cardiace prin cresterea influente simpatikoadrenalovyh. Caracterizat printr-o creștere a frecvenței și puterea contractiilor.
Simpatic infarctul inervația † efectuat terminații Axon neuronilor adrenergici ai gâtului cervicale superioare, de mijloc și stelat (cervical-toracica) Ganglionii.
† Activarea nervilor simpatici produce un efect inotrop pozitiv. frecvență crescută a membranelor depolarizării spontane stimulatoare cardiace care dețin impulsuri este facilitată în fibrele Purkinje. creșterea frecvenței și forța de contracție tipică cardiomiocite.
† acțiunea catecolaminelor asupra cardiomiocite prin 1 adrenoceptori datorită unui număr de evenimente ulterioare: agoniști adrenoreceptori stimulare adrenoceptor (de exemplu, noradrenalina) prin G-proteina adenilciclazei activat pentru a forma activarea fosforilării protein kinazei AMPc-dependentă cAMP sarcolemei proteină p27 este crescută în sarcoplasma intrarea calciului prin deschise voltaj-dependente de Ca2 + -channels îmbunătățită indusă de calciu mobilizarea Ca2 + în citosol prin receptorii ryanodine activat în capac koplazme crește semnificativ concentrația de Ca2 + Ca2 + legare la troponină C tropomyosin ameliorează efectul inhibitor asupra interacțiunii actinei cu miozina produce mai multe actomiozin obligațiuni crește reducerea puterii.
Kompensatornayagiperfunktsiyaserdtsa
Funcționarea mecanismelor menționate mai sus furnizează suplimentar funcției contractile de plată a miocardului deteriorate sau supraîncărcat. Aceasta este însoțită de o creștere substanțială și mai mult sau mai puțin pe termen lung în intensitatea funcționării inimii - hiperactivitatea compensatorie.
Kompensatornayagipertrofiyaserdtsa
hiperfuncția miocardica determină expresia cardiomiocitelor gene individuale. Ea se manifestă o creștere a intensității sintezei acizilor nucleici și proteinelor. Accelerarea sintezei acizilor nucleici și proteinelor miocardului conduce la o creștere a masei sale - hipertrofie. Semnificația biologică a hipertrofia compensatorie a inimii constă în faptul că o funcție crescută a corpului executa greutatea sa a crescut.
Mehanizmydekompensatsiigipertrofirovannogoserdtsa
Potențialul miocardului hipertrofiat și de a crește puterea și de a reduce viteza nu este nelimitată. În cazul în care inima continuă să funcționeze o sarcină crescută sau este deteriorat în continuare, puterea și viteza căderii sale ratei, și crește lor de energie „cost“: dezvoltarea decompensării inima hipertrofiate.
Mecanisme decompensarea inimi hipertrofiate sunt prezentate în Fig. 22-26.
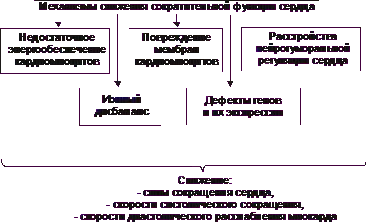
Fig. 22-26. Mecanismele de bază ale decompensării cardiace hipertrofiate.
În centrul decompensare lung miocardului hipertrofiat este o încălcare a unei creșteri echilibrate în diferite structuri sale. Aceste schimbări - împreună cu celălalt (vezi Figura 22-26.) - determină în cele din urmă o scădere a ritmului cardiac și forța ratei contractile a procesului, adică, - dezvoltarea insuficienței cardiace.
Cell-molekulyarnyemehanizmyserdechnoynedostatochnosti
Reducerea funcției contractile a inimii este rezultatul insuficienței cardiace de diverse etiologii. În ciuda diferenței cauzele și particularitatea cunoscute de patogeneza inițială a insuficienței cardiace, a mecanismelor sale de la un singur nivel celular și molecular. Principalele dintre aceste mecanisme sunt prezentate în Fig. 22-27.

Fig. 22-27. Principalele mecanisme de reducere a funcției contractile miocardice în insuficiența cardiacă.
• Lipsa celulelor miocardice de alimentare cu energie
aprovizionare Supărat de procese de bază care au loc în celulele miocardice (in primul rand de contractie si relaxare acestuia), se dezvoltă ca urmare a unor încălcări: macroergs resinteza, transportul energiei lor la structurile efectoare ale cardiomiocitelor, utilizarea energiei a compușilor de fosfat cu energie ridicată. Aceste patogenia, în general, discutate în Capitolul 4, „celule de patologie“ (a se vedea „mecanisme generale de daune“, subsecțiunea „tulburări ale celulelor de alimentare cu energie).
Încălcarea de a furniza energie pentru a cardiomiocitelor etape ale producției, transportului și de eliminare poate fi un mecanism de pornire pentru reducerea funcției contractile a inimii, precum și un factor important în creșterea depresiei sale.
• Deteriorarea membranelor și enzime cardiomiocite
Deteriorarea membranelor celulare și a enzimelor discutate în Capitolul 4, „celule Patologie“ (a se vedea „mecanisme generale de daune“, subsecțiunea „Deteriorarea membranelor și enzime“).
Alterarea membranelor și enzime ale celulelor miocardice - link-ul principal, și de multe ori a INIȚIALĂ patogeneza insuficienței cardiace. Modificări în proprietățile fizico-chimice și conformația ale moleculelor de proteine (structurale și enzime), lipide, fosfolipide și PL, însoțite de reversibilă și adesea semnificativ - leziuni ireversibile ale structurii și funcției membranelor și enzime, inclusiv - mitocondriile, reticulul sarcoplasmic, myofibrils, membranei plasmatice, asigurarea punerii în aplicare a funcției contractile a inimii și ritmul.
Raport și rapoarte între ionii individuali din interiorul si exteriorul celulelor sunt discutate în Capitolul 4, „celule Patologie“ (a se vedea „mecanisme generale de daune“, subsecțiunea „dezechilibru ionic și apă într-o cușcă“). Mai jos sunt specifice pentru dezvoltarea insuficienței cardiace dezechilibru în special de ioni.
dezechilibru ionic în insuficiența cardiacă manifestă raportul încălcare între ionii individuali din diferitele sectoare ale cardiomiocite: in organite (mitocondrii, myofibrils reticulului sarcoplasmic) în citosol, pe partea opusă a membranei plasmatice a cardiomiocitelor. Pentru cea mai mare măsură se referă la ionii: K +. Na +. Ca 2+. Aceste cationi sunt determinate în principal de punerea în aplicare a proceselor, cum ar fi excitație, electro-conjugare, contracția și relaxarea miocardului.
• Perturbări în programele genetice ale cardiomiocite
Violarea in programul genetic al celulelor și / sau a mecanismelor de implementare a acestuia sunt discutate în Capitolul 4, „Patologia celulei“ ( „mecanisme comune de deteriorare“, subsecțiunea „Disorders genetice“).
In insuficienta cardiaca activarea genelor care controlează procesele actualizeze structurile subcelulare ale cardiomiocitelor, precum și o creștere microvasculare și fibrele nervoase. În special, leziuni ischemice și de stres suprimat expresia ARNm pentru Ca 2+ ATPase -dependente reticulul sarcoplasmic. Această inhibare potențează captare și procesul de eliberare reticulul Ca 2+ miocite. În condiții de ischemie și infarct miocardic, stres emoțional cronic suprimat durerea ca procesul de traducere a informației genetice. Aceasta este însoțită de o încălcare a sintezei diferitelor proteine celule miocardice.
• tulburări de reglementare neuroumoral a inimii
Caracteristici generale ale încălcării reglarea funcțiilor celulare, se referă la capitolul 4, „Patologia celulei“ ( „mecanisme comune de deteriorare“, subsecțiunea „Tulburări ale reglementării proceselor intracelulare“). Următoarele sunt considerate importante pentru dezvoltarea insuficienței cardiace, modificări în reglementarea simpatic și parasimpatic a inimii.
† Schimbarea mecanismelor de reglementare simpatic.
‡ Reducerea simpatic neurotransmitatorului sistemului nervos - noradrenalina in tesutul cardiac.
Cauze. Reducerea sintezei noradrenalinei în neuronii sistemului nervos simpatic (acesta normal de format aproximativ 80% din mijlocitorul conținută în miocard). Acesta este rezultatul supresiei activității enzimei tirozin-hidroxilazei și inhibarea absorbției noradrenalinei de terminații nervoase.
‡ Reducerea proprietăților adrenergice a inimii, de exemplu, ino- severitate, cronologică, Drome si norepinefrina bathmotropic si epinefrina.
† schimbarea mecanismelor de reglementare parasimpatic.
Acetilcolina ‡ prin receptori m colinergic determină o scădere a frecvenței cardiace, inhibarea formării de cAMP și cGMP formarea de activare. cGMP activează activitatea de inhibare a kinazei dependentă de cGMP de voltaj-dependente de Ca2 + -channels.
‡ Modificarea Regulamentului parasimpatic a mecanismelor de insuficienta cardiaca este semnificativ mai mică decât simpatic. Acesta este rezultatul unei rezistențe mai mari a mecanismelor parasimpatici diferiților factori dăunătoare.
Consecințele unei încălcări a efectelor simpatic și parasimpatic asupra miocardului este de a reduce gradul de control și fiabilitate a reglementării inimii. Acest lucru duce la o scădere a ritmului și amploarea mobilizării funcției contractile a inimii, în special în condiții de urgență.