hidrocarburi aromatice
hidrocarburi aromatice (arena) - unei molecule de hidrocarburi din care conțin unul sau mai multe inele benzenice. Formula generală a hidrocarburilor aromatice - CnH2n-6.
Cel mai simplu reprezentant al hidrocarburii aromatice este benzen - C6 H6
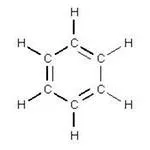
Conform conceptelor moderne de atomi de carbon în benzen sunt în sp2 hibridizare. Este stabilit că toți electronii sunt implicați în formarea de legături între atomii de carbon din benzen distribuite uniform. Fiecare atom de carbon este legat la două sp adiacente 2 prin electroni și p-electroni. nor P-electron optari în vrac în formă situate perpendicular pe planul molecular și uniform se suprapun unul cu celălalt și formează un sistem unic π-electron. Acest amestec special de șase legături cu un singur sigma sistem numit π- legătură aromatică.
Denumirile produc hidrocarburi aromatice prin cuvintele „benzen“ sau „fenil“, de exemplu, metilbenzen, fenilmetansulfanilamino toluen.
Dacă există 2 substituenți în moleculă benzen, ele reprezintă "orto-" (o-, 1,2) "m-" (M, 1,3), "para" (n, 1,4 -)
Metodele de preparare a arenelor.
În principal, hidrocarburi aromatice obținute din produsul de distilare a cărbunelui și petrolului. Sintetic le-a produs:
2. Dintre sărurile acizilor aromatici:
3. Prin reacția Friedel-Crafts a Omologii benzen obținut:
4. Reacția de Vyurtsa- Wilhelm Rudolph Fittig:
Proprietățile chimice ale hidrocarburilor aromatice
Aderarea 1. hidrogen:
2. halogeni aderare:
3. Înlocuirea unui atom (sau atomi) halogen hidrogen (e):
6. Alchilarea (reacția Friedel-Crafts):
7. Oxidarea. Benzenul este rezistent la oxidare, homologs de benzen, de exemplu toluen oxidanți puternici este oxidat la acid benzoic (K2 Cr2 O7 KMnO 4.):
Termenii de orientare în timp ce reacțiile de substituție electrofilă în derivați de benzen.
Densitatea de electroni uniformă în molecula de benzen este de obicei rupt cu anumiți deputați. al doilea substituent este ghidat într-o poziție definită la primul în reacții de substituție electrofilă (SE).
Substituenți (orientant) de primul tip sunt electroni și hrănite reintroducând substituenților la poziția orto și para față de ea însăși. Acestea includ: -N (CH3) 2, -NH2, -OH, -CH3. CI, Br. și altele.
Substituenți (orientant) al doilea tip sunt electroatractor și re-intră substituenții direcți în poziția meta față de ea însăși. Orientant Acestea sunt: - NO2. -C ≡ N, - COH, -COOH, - SO3 H.
A fost o lecție în chimie 33 - hidrocarburi aromatice. Benzenul. Prepararea, proprietățile