Comportamentul materiei în imponderabilitate
Comportamentul materiei în imponderabilitate
Statele agregate și fază ale substanței. Având în vedere comportamentul materiei în spațiu sunt termeni, cum ar fi componentele de agregare și de stat fază și fază utilizate în mod frecvent. Să ne definim aceste concepte.
stare agregată a materiei disting prin natura mișcării termice a moleculelor sau atomilor. De obicei, ei vorbesc despre cele trei stări de agregare - gazoase, lichide și solide. Moleculele de gaz sunt aproape niciodată asociate forțele de atracție și să circule liber, umple intregul vas. Structura solidelor cristaline se caracterizează prin rânduială înaltă - atomii sunt aranjate în rețea cristalină lângă care fac fluctuații numai termice. Ca rezultat, solide cristaline au o formă strict limitată, iar atunci când încercați să-l modifice într-un fel, există forțe elastice considerabile a contracara o astfel de schimbare.
Împreună cu cristale cunoscute și un alt tip de solid - corp amorf. Caracteristica principală a structurii interne a solidelor amorfe - lipsa totală de ordine: numai în aranjamentul atomilor învecinate, procedura care se înlocuiește cu aranjament aleatoriu una față de cealaltă, la distanțe mai mari. Cel mai important exemplu de stare amorfă - această sticlă.
Aceeași proprietate - ordinul de rază scurtă de acțiune în aranjamentul atomilor învecinate - are o substanță în stare lichidă. Din acest motiv, modificarea volumului lichidului nu provoacă să aibă forțe elastice semnificative, și în condiții normale de lichid ia forma vasului în care se află.
În cazul în care substanța este format din mai multe componente (elemente chimice sau compuși), atunci proprietățile sale depind de concentrațiile relative ale acestor componente și temperatura, presiunea și alți parametri. Pentru caracteristicile produsului final, formate prin combinarea acestor componente, se utilizează conceptul de fază. În cazul în care substanța în cauză constă în invecineaza reciproc părți omogene, proprietățile fizice sau chimice ale care sunt diferite, aceste părți sunt numite faze. De exemplu, un amestec de gheață și apă este un sistem de două faze, și apă, în care aerul dizolvat, - o singură fază, pentru că în acest caz, nu există nici o interfață între componentele.
Faza de stat - un concept bazat pe reprezentarea structurală a termenului „faza“. Starea de fază a materiei este definită numai prin natura aranjamentului mutual a atomilor sau moleculelor și nu mișcarea lor relativă. Prezența comenzii pe distanțe lungi (comanda completă) corespunde fazei cristaline de stat, ordinea rază scurtă de acțiune - starea de fază amorfă, o lipsă totală de ordine - starea de fază gazoasă.
Faza de stat nu coincide neapărat cu agregatul. De exemplu, starea de fază amorfă corespunde unei o stare lichidă normală și o stare solidă sticloasă. în stare solidă corespunde cu două faze - cristalină și amorfă (sticlos).
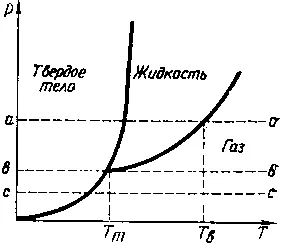
Fig. 2. Sistemul Diagrammar Travnovesiya-component
Tranziția unei substanțe de la stat o etapă la alta se numește o tranziție de fază sau transformare. Dacă două sau mai multe faze diferite ale substanței la o anumită temperatură și presiune există simultan în contact unul cu altul, atunci vorbim de un echilibru de fază. Fig. 2 prezintă un exemplu de diagrama de faza de echilibru a unui sistem cu un singur component, pe baza presiunii (p) - temperatura (T). Acolo izobară (adică presiune constantă directă ..) Aa corespunde tranzițiilor directe solide - lichid (topire și solidificare) și lichid - gaz (evaporare și condensare), izobata cu cu - tranziție solid - gaz (sublimare), și izobară într-un - toate cele trei faze coexistă în așa-numitul punct triplu, la anumite valori ale lui p și T.
Efectul microgravitatie asupra lichidului. Cum gravitația asupra comportamentului materiei în diferite stări de agregare? In solide, atomii și moleculele sunt aranjate în ordine strictă, iar forța de gravitație nu poate avea un impact semnificativ asupra proceselor care au loc în această stare.
Pe procesele din gazele care puterea pot afecta în mod semnificativ mai mult. Este cunoscut, de exemplu, că în condițiile de încălzire neuniformă a diferitelor straturi ale gazului în atmosferă are loc prin forța de gravitație prin convecție liberă, adică. E. Un comandat schimb de gaz între straturi. In conditii fara greutate nu se poate produce acest efect.
Dar o forță de impact deosebit de puternic de greutate exercită asupra fluidului. În trecerea la lichidul în imponderabilitate dispare forța lui Arhimede care acționează asupra componentelor diferite de densitate și care duce la separarea lor, schimbarea naturii curenților de convecție rolul relativ al interacțiunilor intermoleculare în lichid și devine posibil să se dețină liberă în afara vasului (fenomenul de levitație). Luați în considerare aceste motive mai multe procese în lichid.
Ca și în cazul moleculelor de gaz în lichid nu a fost stabilită, dar din cauza mută de energie termică din loc în loc. Dacă, în orice loc al particulelor lichide ale unei specii predomină, apoi datorită coliziunilor mai frecvente între ele trec treptat într-o zonă în care concentrația lor este mai mică. Acest proces se numește difuzie. Deoarece timpul de difuzie t peste particula este deplasată printr-o distanță x = (2DT) 1/2. unde D - coeficientul de difuzie. Dacă luăm în considerare particula ca o sferă de rază r. atunci D = W · (?? r) -1. Aici W - energia termică a particulelor. - vâscozitatea fluidului, care este foarte dependentă de temperatura. Când lichidul este răcit, vâscozitatea crește și astfel încetini procesul de difuzie.
Dacă modificarea concentrației unui tip de particule la o distanță? X în lichid este egal? A. apoi printr-o unitate de suprafață de la 1 la numărul de particule trebuie să treacă I = - D c / x ??.
În unele cazuri, lichidul poate conține componente de densitate variabilă. Pe Pământ, sub acțiunea forțelor se face treptat Arhimede separarea acestor componente (de exemplu, smântână și lapte degresat sunt formate). În această imponderabilitate separare Nu contează cu proprietăți unice pot fi obținute după solidificare a lichidelor. Lichidul poate cuprinde faze care nu sunt miscibile între ele, de exemplu, kerosen și apă. Pe Pământ, printre ei au format o limită clară. In microgravity poate fi obținut prin amestecarea amestecului stabil, format din mici picături de ambele faze. După solidificare a unor astfel de amestecuri de faze diferite, se pot obține compozite omogene, spume de metal și altele asemenea. N.
Apariția interfețelor dintre diferitele faze în fluidul datorită prezenței tensiunii superficiale sau forța capilară care apare datorită interacțiunii dintre moleculele de lichid. Tensiunea superficială poate fi comparată cu o forță care resetează șirul atunci când muzicianul încearcă să-l tragă în lateral. Este tensiunea superficială conduce la ceea ce este rău din macara închis picături toamna, și nu a turnat un flux subțire de apă. Dar pe Pământ picăturile sunt mici: forța gravitațională este mult mai mare decât tensiunea de suprafață și se rupe în bucăți prea mari dintre ele. În imponderabilitate, nimic nu poate preveni formarea de picături foarte mari, iar corpul de lichid, la stânga la sine, ar lua o formă sferică.
De fapt, nava spatiala din cauza diferitelor tipuri de accelerațiilor mici stare de imponderabilitate deranjat. Dacă r - raza sferei, care ia forma unui lichid, apoi acționează pe ea este egală cu forța capilară de aproximativ r ?. în cazul în care. - coeficientul de tensiune superficială. Amploarea forțelor care acționează asupra masei inerțiale cu masa lichid este? Gr 3. în cazul în care. - densitatea lichidului, g - o accelerație scăzută. Evident, efectele tensiunii superficiale, va juca un rol important atunci când. · (? Gr 2) -1> 1. Această condiție este determinată de posibilitatea de a obține într-o stare aproape de zero gravitație, a sferelor de lichid cu o rază r. O astfel de sferă de lichid la bordul navei spațiale poate fi într-o stare de plutire liberă, pentru a le reține atunci când nu este nevoie de nave. Dacă această topitură de lichid se solidifică atunci când contaminanții din lume vine de pe pereții vaselor. În spațiu, puteți face fără a navei și, prin urmare, pentru a primi mai multe substanțe pure.
Se încălzește și de transfer de masă în imponderabilitate. tranziție impact semnificativ imponderabilității oferă, de asemenea procese de transfer de căldură și de masă în lichide și gaze. Transferul de căldură poate fi conductivitate termică, convecție sau radiație precum și orice combinație a acestor mecanisme. Conductivitatea termică - un proces de transfer de căldură din zona cu o temperatură mai mare în zona în care temperatura este mai scăzută prin difuzia moleculelor din mediul dintre aceste zone. Din acest motiv, conductivitatea termică este proporțională cu coeficientul de difuzie.
Radiații de transfer de căldură caracteristic principal pentru solide și lichide și are loc la temperaturi suficient de ridicate. Procesele de transfer de căldură radiativ și conductivitate termică nu depind de forța de gravitație, sau de către forțele care acționează în masă mici la bordul navei spațiale.
Situația este diferită de transfer convectiv de căldură. Convectie - un transfer de căldură într-un mediu lichid sau gazos prin mișcarea macroscopică a unei substanțe naturale de mediu. Deja citat mai sus simplu exemplu convecția - liber (sau natural) prin convecție se produce datorită distribuției temperaturii inegale în mediu, supus acțiunii forțelor de masă (de exemplu, gravitatea sau forțele de inerție cauzate de accelerații în nave spațiale mici). Acest fenomen se poate observa cu ușurință la domiciliu, în orice reincalzitor unde straturile de lichid având o temperatură mai mare și, prin urmare, o densitate mai mică, va pluti în sus și transporta cu ea caldura, iar în locul lor pe refierbătorul fund fierbinte va coborî mai mult straturi reci și dense.
Rolul relativ al transferului de căldură prin convecție liberă și conductivitatea termică este determinată de numărul Rayleigh:
În cazul în care g - accelerația care acționează asupra sistemului, L - dimensiunea caracteristică a sistemului. - coeficient de dilatare volumetric, T - scădere a temperaturii în mediu. - coeficientul de conducție termică. - vâscozitatea mediului. Aceasta implică faptul că, în condiții care se apropie de zero gravitate (g> 0), Ra> 0 și, prin urmare, rolul de convecție, ceea ce duce la mediu o amestecare eficientă, poate fi neglijată.
Această concluzie are o dublă semnificație. În primul rând, contribuția redusă a convectie în procesul de transfer de căldură, și transferul de căldură este mai lent proces de conducție a căldurii. În al doilea rând, eliminarea curenților de convecție în mediul conduce la faptul că rolul principal în transferul de masă va juca nici o mișcare procese de difuzie și substanțe macroscopice. Aceasta, la rândul său, se deschide posibilitatea de a produce substanțe în care distribuția impuritate este mult mai uniformă decât în lume.
În plus față de convecție liberă, există o serie de alte efecte de convecție, dintre care unul depinde de forțele de masă, iar celălalt nu. De asemenea, cunoscut convecție forțată care are loc sub influența oricărui factor extern (de exemplu, mixere, pompe și așa mai departe. P.). In acest tip de condiții de spațiu convecție este utilizată pentru a asigura viteza necesară de îndepărtare a căldurii din unitățile operaționale.
Ca un exemplu, convectie, nu depinde de forțele de masă, subliniem Thermocapillary convectie care rezultă din faptul că la limita fazei lichide se poate produce și propaga valuri. valuri capilarelor cauzate de schimbările de temperatură, din care, din cauza valorii tensiunii de suprafață nu este constantă de-a lungul suprafeței. Acest tip de curenți de convecție, în mod evident, nu depinde de valoarea g și poate conduce la o deteriorare a omogenității materialelor obținute în spațiu. O metodă de compensare a efectelor nocive ale acestui efect este de a reduce schimbările reale de temperatură de-a lungul interfeței.