Capacitatea de căldură - Enciclopedia fizică - Enciclopedia & Dicționar
cantitatea de căldură absorbită de corpul uman atunci când este încălzit 1 grad (1B ° C sau 1 K); să fie exact - raportul dintre numărul de căldură absorbită de către organism din cauza unei schimbări în infinitezimal său rata de riu, la această schimbare. Unități T.. greutate wa (r, kg) este numit. specific Volumul 1 mol în Insulele - mol (mol) T. Ed. T. servi J / (kg • K) J / (mol • K), J / (m 3 • K) și unitățile off-sistem. cal / (mol • K).
Cantitatea de căldură absorbită de organism atunci când modificările de stat nu depinde numai de stările inițiale și finale (în special, asupra ratei lor de-riu), dar, de asemenea, pe cale de a-ochi a fost efectuat tranziția între ele. Prin urmare, metoda de încălzire depinde de corp si sunt de obicei distinse T. T. în post. Volumul (cv) și T la post. presiune (cp), dacă este menținut constant în mod corespunzător volumul sau presiunea acestuia în procesul de încălzire. Prin încălzirea la post. presiune de căldură se duce la producerea lucrărilor de extindere a corpului, iar unii - pentru a crește energia internă, în timp ce încălzirea la post. volumul toată căldura consumată pentru a crește ext. energie; în acest sens, cp este întotdeauna mai mare decât CV-ul. Pentru gaz (diluat, astfel încât acestea pot fi considerate ideale) diferența cf. T. mole-cv = R, unde R - Univers. gaz constantă egală cu 8.314 x D / (mol • K), sau 1,986 cal / (mol • K). În lichide și TV. tel diferența dintre cp și CV-ul este relativ mic.
Din 1 și 2 au început termodinamicii care av = T (dS / dT) p și cv = T (dS / dt) v, m. E. T. proporții. derivat al entropia S pentru T D-paced sistem în condiții adecvate.
Teor. calcularea TA, în special, în funcție de corpul său rata de riu nu poate fi realizată printr-o pur termodinamic. metode și necesită aplicarea metodelor fizicii statistice (țintă de cunoștințe microstructura). T. Pentru gazele de calcul se reduce la calculul Wed. termică Dep energie mișcare. molecule. Această mișcare este formată din postupat. și vârtejul. mișcări ale moleculei în ansamblu și a oscilațiilor atomilor din moleculă. Potrivit clasice. Statisticile postupat pentru fiecare grad de libertate. și vârtejul. mișcări au un T. molar (cv) din cantitatea de gaz egal cu R / 2, și fiecare kolebat. gradul de libertate - R; este de obicei numit. legea echipartiție. B-ca gaz monoatomic are doar trei postupat. grade de libertate, respectiv, ar trebui să fie T. cv 3R / 2 (t.e.ok. 12,5 J / (mol • K) sau 3 cal / (mol • deg)), în bună concordanță cu experimentul. molecula de gaz diatomica are trei translațională, doi vârtejul. și unul kolebat. grade de libertate și legea echipartiție duce la cv value = 7R / 2; Experiența arată că T. mol de gaz diatomic (cel normal de ritm-pax) este 5R / 2. Oto discrepanță între teorie și experiment se datorează faptului că, în calculul T ar trebui luate în considerare efectele cuantice, adică. E. Utilizarea statisticilor cuantice. Potrivit mecanicii cuantice, fiecare q sistem h, oscilații care efectuează sau rotații (r. H. Molecula de gaz) poate avea numai anumite valori energetice discrete. În cazul în care energia de mișcare termică în sistem nu este suficient pentru excitarea unei anumite vibrații de frecvență, aceste vibrații nu contribuie la sistemul T. (corespunzător gradului de libertate este „înghețat“ - nu este aplicabilă echipartiție lege). Temp T, realizând în același timp o lege roi echipartiție se aplică învârtească. sau kolebat. gradul de libertate este determinată de-mecanică cuantică. raportul dintre T -> hn / k, unde n - frecvența de oscilație.
Intervalele dintre vârtejul. nivelele de energie ale unei molecule diatomice (împărțit la k) reprezintă doar câteva. K și numai pentru astfel de molecule de lumină ca molecula de hidrogen, ajunge la sute de K. Prin urmare, atunci când rata normala rah-vârtejul. T. parte dihidroalcool (și polihidroxilic) de gaz echipartiție se supune legii. Intervalele dintre kolebat. nivelurile de energie ajunge la mai multe. Prin miile, și, prin urmare, la o lege normală ritm-Rah echipartiție nu este aplicabilă kolebat. Calcularea T. T. statisticilor cuantice conduce la rezultatul că kolebat. T. scade rapid cu scăderea tempo-riu, care tinde spre zero. Aceasta explică faptul că, chiar și la ritmul normal de-rah kolebat. porțiunea T. este practic absentă și T. mol gaz diatomic este 5R / 2 în loc de 7R / 2.
La suficient de scăzută rata pax T., în general, trebuie să fie calculată utilizând statisticile cuantice. După cum se dovedește, T. scade odată cu scăderea ratei-riu la zero la T V®0 în acord cu m. N. Principiul Nernst (a treia lege a termodinamicii).
În televizor. (Cristalin). Organele mișcării termice a atomilor este o anumite mici oscilații lângă poziții de echilibru (nodurile cristae.) Grile. Fiecare atom are m. O. trei kolebat. grade de libertate, și, în conformitate cu legea echipartiției, Mole T. TV. Corpul (. T. cristae zăbrele) trebuie să fie egal 3nR, unde n - numărul de atomi în moleculă. În realitate, însă, această valoare - limita doar la a-rom caută T. TV. corp la ritmul alert-Rah. El a ajuns la ritmul obișnuit-rah în multe altele. elemente metalice inclusiv (n = 1, t n Dulong și Petit lege ..) y anumitor compuși simpli (NaCl, MnS (n = 2), PbCI2 (n = 3), etc.) ...; în compuși complecși, de fapt, nu se atinge această limită, adică. k. înainte de a se produce topirea în insulele sau descompunerea acesteia.
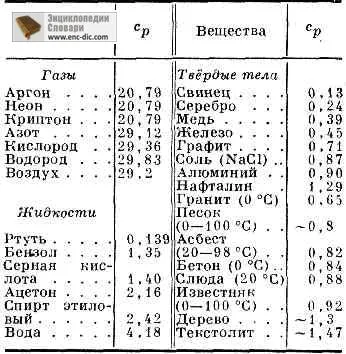
cp căldura specifică a anumitor gaze (în J / (mol • K), lichide sau solide (în kJ / (kg • K) ATM AT. Presiunea la t = 25C ° C
La nivelul temp-rah, componenta zăbrele T. TV. corp se transformă raportul. abs cub. ritmul-riu (capacitate termică Debye a legii). Criteriul de a distinge între înaltă și joasă temperatură-riu, yavl. compararea lor cu caracteristicile fiecăreia dintre insulele din - așa-numitul caracteristică, sau Debye ritm roi Qd. Această valoare este determinată de atomii de spectru oscilație în organism și, astfel, depinde în mod esențial pe cristae acestuia. structura (a se vedea. VIBRATIILOR rețea cristalină). De obicei, 6D - de ordinul mai multor. Pentru celule, dar poate ajunge (de ex. Un diamant) și mii de K (vezi. Temperatura Debye).
În metale, o anumită contribuție la televizor este, de asemenea, furnizate și e-mail-conducția (de ex., N. E-TS). Această parte a TA poate fi calculată folosind statistici cuantice Fermi, un roi Supuneți de e-HN. E T. proporție din metal. primul grad abs. ritmul-riu. Este, cu toate acestea, valoare relativ mică, contribuția sa la T. de metal devine semnificativă numai atunci când rata de pax aproape de abs. zero (aproximativ mai multe. K), zăbrele când T (= T3) devine neglijabilă. Kristen. organisme cu un aranjament ordonat de magnet de spin. momente ale atomilor (materiale feromagnetice și antiferomagnetice), există completeze. magnet. componenta T. Atunci când rata de re paramagnetic fază de tranziție în. stat (la punctul Curie sau, respectiv, punctul Neel), această componentă suferă o creștere accentuată T. -nablyudaetsya „vârf“ care T. yavl. o trăsătură caracteristică a tranzițiilor de fază de tip II.
motoarele de căutare Ajutor