Apă și gheață în natură
3. o apă de 1000 kg / m3) gheața plutește pe apă. Cu o conductivitate termică scăzută, stratul protejează apă rece ca gheața prezentă sub ea, prin răcire și congelare. Prin urmare, pește și alte creaturi vii în apă, nu mor în timpul îngheț. Dacă gheața sa scufundat, ea nu este ape foarte adânci ar fi inghetate prin iarna prin.
După extinderea înghețarea apei într-un recipient închis, există forțe uriașe care se pot sparge mingea cu ziduri groase de fier. O astfel de experiență este ușor de implementat cu o sticlă umplut de gât și expuse la apă rece. Pe suprafața dopului de gheață de apă formată, sticla înfundare, iar sticla este rupt la expansiunea congelare a apei.
Înghețarea apei în crăpăturile de roci duce la distrugerea lor.
Capacitatea apei de a extinde timpul de solidificare trebuie luate în considerare la montarea conductelor de apă și de canalizare și de încălzire a apei. Pentru a evita ruperea în timpul înghețării conductelor subterane de apă trebuie să fie amplasate la o astfel de adancime încât temperatura nu a căzut sub O ° C Părțile exterioare ale țevilor trebuie să fie suportate în materialele de iarnă izolatoare.
Dependența punctului de topire al presiunii asupra
Dacă topirea materialului este însoțită de o creștere a volumului său, apoi prin creșterea presiunii externe mărește punctul de topire al substanței. Acest lucru poate fi explicat după cum urmează. substanța Compression (cu creșterea presiunii externe) împiedică creșterea distanței dintre moleculele și, prin urmare, crește energia potențială a interacțiunii moleculare, care este necesară pentru tranziția la starea lichidă. Prin urmare, este necesar să se încălzească corpul la o temperatură mai ridicată, în timp ce potențialul moleculele de energie nu ating valoarea dorită.
Dacă topirea materialului însoțită de o reducere a volumului său, apoi prin creșterea presiunii externe a temperaturii de topire scade.
De exemplu, gheața la o presiune de 6 x 10 7 Pa topește la -5 ° C și la o presiune de 10 Pa × 8 Temperatura 2.2 topirea gheții este -22 ° C
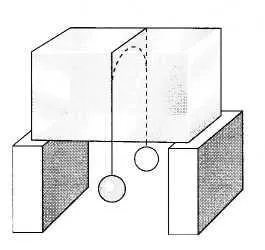
Coborârea punctului de topire a gheții este bine ilustrată de experiență cu presiune crescătoare (fig. 8.34). fir de nailon trece prin gheață fără să-l distrugă. Faptul este că, datorită presiunii semnificative asupra firului se topește gheața de sub ea. Apa, care curge de sub filament, apoi re-ingheata.
punctul triplu
Lichidul poate fi în echilibru cu vaporii săi (abur saturat). În figura 6.5 (a se vedea. § 6.3) prezintă dependența presiunii de vapori la temperatură (curba AB) obținută experimental. Deoarece fierberea are loc atunci când presiunea lichidului egal cu vaporii de saturație, această curbă dă dependența de temperatură a punctului de fierbere la presiune. Regiunea situată sub curba AB, se întâlnește cu gaz a, și deasupra - lichid.
Solidele cristaline sunt topite la o anumita temperatura la care faza solidă este în echilibru cu lichidul. Temperatura de topire depinde de presiune. Această relație poate fi prezentată în aceeași figură, care arată dependența punctul de fierbere la presiune.
Figura 8.35 TC Curba caracterizează dependența punctul de fierbere al presiunii. Se termină la punctul K corespunzătoare temperaturii critice, deoarece peste această temperatură lichid nu poate exista. Left TC curba prin punctele experimentale se construiește curba de temperatură TC topire în funcție de presiunea (spre stânga, ca fază solidă corespunde la o temperatură mai scăzută decât lichidul). Cele două curbe se intersectează într-un punct T.
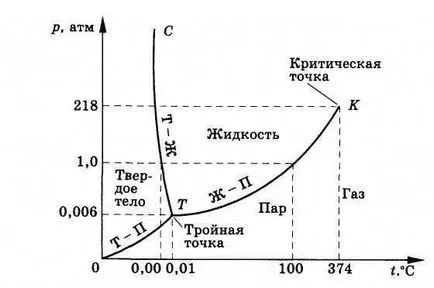
Ce se întâmplă cu substanța la o temperatură mai mică decât temperatura ttp corespunzând unui punct T? nu poate exista deja Faza lichidă la această temperatură. Substanța este un solid sau un gaz. Curba de la (.. A se vedea figura 8.35) corespunde stările de echilibru ale solid - gaz care apar în timpul sublimarea solidelor.
Trei curbe CT și OT TC planul de fază este împărțită în trei regiuni în care materialul poate fi într-una din cele trei faze. Curbele Sami descriu stările de echilibru ale lichidului - vapori, lichid - perechi - solide și solide. Există doar un singur punct T, în care toate cele trei faze sunt în echilibru. Acesta este triplu punct.
Punct triplă corespunde unei temperaturi și presiune unică. Acesta poate fi reprodus cu acuratețe, și este una dintre cele mai importante puncte de referință în construcția scalei temperaturii absolute. Pentru apa, temperatura absolută a punctului triplu luat ca TET = 273,16 K sau ttp = 0,01 ° C
Figura 8.35 arată diagrama de fază a apei, în care temperatura de topire scade cu o presiune tot mai mare. Pentru substanțele convenționale curba TC este înclinată în direcția opusă față de trecerea verticală prin punctul T.
De exemplu, acest tip va avea o diagramă de fază de CO2 de dioxid de carbon. Temperatura punctului triplu al SO2ttr = -56,6 ° C și presiune = 5,1 atm ptr. Prin urmare, la presiunea atmosferică normală, la o temperatură apropiată de temperatura camerei, dioxidul de carbon poate să nu fie în stare lichidă. CO2, Faza solidă este, în general, cunoscut sub numele de gheață uscată. Are o temperatură foarte scăzută și nu se topește și se evaporă imediat (sublimare).
Modificarea volumului în timpul topirii și solidificării este direct legată de dependența punctului de topire la presiune. Marea majoritate a substanțelor punctul de topire crește cu presiune. În apă și alte substanțe este, dimpotrivă, scade. Pentru locuitorii Pământului la latitudini mari, este o mare binecuvântare.
Există un punct unic pe diagrama p -T (triplu punct), în care toate cele trei faze ale unei substanțe sunt în echilibru.
In concluzie Fizica esențiale Solid State pentru dezvoltarea tehnologiei și a civilizației, în general.
Omenirea a folosit întotdeauna și va folosi solide. Dar, dacă înainte de fizica în stare solidă, nu ține pasul cu dezvoltarea tehnologiei bazate pe experiența directă, dar acum situația sa schimbat. Studiile teoretice încep să conducă la crearea de solide ale căror proprietăți sunt destul de neobișnuite și obține prin „încercare și eroare“ ar fi imposibil. Invenția de tranzistori, care va fi discutat mai târziu, un prim exemplu de modul în care o înțelegere a structurii solide a dus la o revoluție în întregul radio.
Dezvoltarea materialelor cu proprietăți mecanice, magnetice și alte specificate - una dintre principalele zone ale fizicii stării solide. Aproximativ jumătate dintre fizicieni din întreaga lume sunt acum lucrează în domeniul fizicii stării solide.